
(6分)【实验探究】
(1)请你依据下图设计一个酸和碱反应的探究实验: 
| 实验步骤 | 实验现象 | 结论 |
| ①向烧杯中加入10mL氢氧化钠溶液,并滴入几滴酚酞试液 ②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液。 | ①溶液颜色 ; ②不断搅拌溶液至溶液颜色变成 色。 | 酸和碱发生了中和反应 |
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 甲同学的方案 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 硫酸过量 |
| 乙同学的方案 | 取样,滴入几滴无色酚酞溶液 | 酚酞溶液不变色 | 酸、碱恰好完全反应 |
| 丙同学的方案 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 硫酸过量 |
【实验探究】(1)实验现象:① 变成红色 ② 无色。
(2)【实验评价】① 丙 ② 硫酸钠溶液也能与氯化钡反应生成白色沉淀 酚酞遇酸也不变色
【实验反思】 Zn
解析试题分析:【实验探究】(1)①无色酚酞遇碱溶液变红色,遇酸溶液不变色,所以向烧杯中加入10mL氢氧化钠溶液,并滴入几滴酚酞试液,溶液颜色变红,②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液,发现溶液变为无色,可得出结论:酸和碱发生了中和反应
(2)【实验评价】①三个方案中只有丙是正确的,另外两个同学方案错误的原因,甲同学错误的原因是:因为溶液中还有生成的硫酸钠,而硫酸钠溶液也能与氯化钡反应生成白色沉淀,所以无法确定是否含有硫酸,乙同学错误的原因:酚酞不仅在中性溶液中不变色,遇酸也不变色
【实验反思】探究硫酸和氢氧化钠反应后硫酸是否有剩余,实际就是抓住硫酸的化学性质,所以还可选择一种试剂活泼金属,如锌或碳酸盐
考点:酸碱的化学性质


科目:初中化学 来源: 题型:问答题
用 Y形管或 Y 形导管完成以下实验。 
(1)图9中Y形管左侧管中加入无色酚酞试液,右侧管中加入浓氨水,一段时间后,可观察到的现象:________________________,用分子的观点解释这一现象:________________________。
(2)图10 中 Y 形导管平放于桌面,实验中可观察到的现象;________________________,用化学方程式解释结论:________________________;若把Y形导管固定在铁架台上(如图 11 ) , a 管位于上方, b 管位于下方,两石蕊试纸均湿润,可观察到 b 管中试纸变色比a 管明显,原因:________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
天然气作为燃料已进入千家万户。小聪在帮助父母烧菜时想到:天然气燃烧的产物是什么呢?带着这一问题,小聪和同学一起进行了如下的探究。
(1)设计与实验:同学们设计了甲图装置(固定装置未画出),将天然气在氧气中点燃后得到的混合气体通过该装置进行实验。开始时应______(填“先通气体”或“先加热”);加热过程中发现黑色CuO固体变红,澄清石灰水变浑浊。写出CuO固体变红的化学方程式__________________。仅根据甲图装置出现的现象,写出混合气体所有的可能组成____________。
(2)评价与改进:小聪认为上述实验方案有缺陷,通过讨论,增加了乙图中的3个装置(固定装置未画出),对方案作了改进并进行实验:将混合气体先通过乙图中连接的装置后,再通入甲图装置。实验中部分现象如下:A装置质量增加,B装置中溶液不变浑浊,甲图装置中实验现象与(1)相同。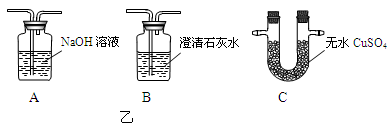
请你写出改进方案的装置连接顺序(装置不重复使用):混合气体→______→甲图装置(填装置编号)。
(3)交流与讨论:通过对改进实验的现象分析,同学们得出了正确的结论。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
定性和定量结合既是化学的重要思想,也是研究物质组成的重要方法。某研究性学习小组为检测实验室用H2还原CuO所得红色固体Cu中是否含有Cu2O(红色),进行了认真的研究。请你一起踏上探究之路,回答下列问题。
【查阅资料】①无水CuSO4遇水变蓝 ②高温灼烧CuO生成Cu2O和O2 ③Cu2O与稀H2SO4反应:Cu2O+H2SO4=Cu+CuSO4+H2O
【设计实验方案】
方案1 取该红色固体加入适量稀H2SO4,实验现象为 ,结论为红色固体中含有Cu2O.
方案2 装置如图所示,拟通过干燥管中CuSO4变蓝来判断红色固体是否含有Cu2O.
(1)为确保探究的科学、合理、安全.实验中还应采取的措施有 ;(填序号)
①加热前先排尽装置中的空气
②在氢气发生器与硬质玻璃管之间加一个干燥装置
③在盛有CuSO4的干燥管后再连接一个装有浓H2SO4的洗气瓶
(2)由方案2实验后得出结论:红色固体中含有Cu2O.写出红色固体Cu2O与H2反应的化学方程
式
方案3 称得干燥坩埚(常用于固体加热的容器)的质量为ag,取红色固体置于坩埚中称得总质量为bg,在空气中高温灼烧至质量恒定,称得最后坩埚与固体总质量为cg.
(1)该实验方案最少得进行 次称量;
(2)若确认红色固体中含有Cu2O,则c与a,b应符合的数学关系式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
实验小组同学向盛有2ml稀硫酸的试管中加入2ml氢氧化钠溶液,未观察到明显现象。
【提出问题】两者是否发生了化学反应?
【实验探究】将盛有上述实验混合液的试管标为①,如图甲。
小华:测得实验所用稀硫酸的pH<7,试管①中溶液pH>7。于是得出结论: 。
小敏:取两支试管,编号为②和③,分别加入稀硫酸和试管①中溶液各2ml,逐滴滴加Na2CO3溶液至过量,实验过程与现象如图乙,由此他得出了与小华一样的实验结论。
【反思评价】小军认为小敏在实验设计中存在不够严密的地方,请帮他指出: 。
【交流讨论】试管③中的溶液中有哪些溶质?同学们分析了两位同学的实验过程,一致认为没有H2SO4,其理由是 。在此基础上,同学们提出了二种推理:
推理1:含有Na2SO4、Na2CO3和NaOH
推理2:含有Na2SO4、Na2CO3
正确的是推理 (选填“1”或“2”)。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验。
①制备氧化铜并检验产物,装置如下图所示(省略夹持仪器):
步骤一:连接A和B,打开活塞,通入空气。
步骤二:关闭活塞,连上C和D,开始加热。
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热。
| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |

查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某化学小组查阅资料得知:在不同温度下,甲烷(CH4)可将氧化铁(Fe2O3)还原为Fe、Fe3O4中的一种可两种。他们为探究甲烷与氧化铁反应后产物(黑色粉末)的成分,进行了如下实验:
(1)按右图装置连接好仪器,检查装置的气密性后,往装置中添加药品。
①各黑色粉末中滴加稀硫酸,观察到有气泡产生,则黑色粉末中含有 ,产生气泡的化学方程式是 。
②导管b的作用是 。
(2)按下图装置连接好仪器(图中夹持设备已略去)检查装置的气密性,往装置中添加药品,打开止水夹K通入含有少量二氧化碳的的一氧化碳,持续一段时间后再点燃装置C处的酒精喷灯。
①装置A中反应的化学方程式为 ,装置B中浓硫酸的作用是 。
②持续一段时间后再点燃装置C处的酒精喷灯的原因是 。D装置的作用是 。
③实验中观察到装置E中石灰水变浑浊,则黑色粉末中含有 。尾气处理方法为 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
(9分)废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如下图所示:
(1)在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外还有: , ;
(2)滤液M中肯定含有的溶质的化学式是 、 ;
(3)在实验室中完成操作A的玻璃仪器有玻璃棒、烧杯和 ;
(4)滤液M经过操作B可得硫酸亚铁晶体(FeSO4·7H2O)。已知硫酸亚铁的溶解度和析出晶体的组成如下表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |
| 析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | ||||||||
查看答案和解析>>
科目:初中化学 来源: 题型:单选题
下列有关物质鉴别方案正确的一组是:
| A.可用Ba(OH)2溶液鉴别(NH4)2CO3、(NH4)2SO4、NH4NO3三种氮肥 |
| B.MgCl2溶液、NaOH溶液、H2SO4溶液、CuSO4溶液,不加任何试剂即可鉴别 |
| C.Na2CO3溶液、Ca(OH)2溶液、盐酸、BaCl2溶液,不加任何试剂即可鉴别 |
| D.CuO粉末、炭粉、铁粉,三种黑色粉末用一种试剂无法鉴别 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com