
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| 纯牛奶 保持期:8个月 净含量:250mL/盒 营养成分:(每100mL) 钙≥0.1lg 脂肪≥3.3g 蛋白质≥2.9g |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题

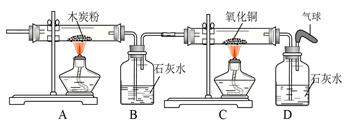
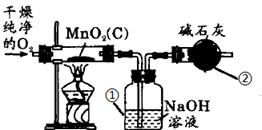
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
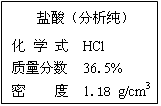
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| 加入氢氧化钠的 溶液的质量/g | 20 | 40 | 60 | 80 | 160 | 180 |
| 生成沉淀的质量/g | 0 | 0 | 0.89 | 1.78 | 5.35 | 5.35 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com