
| A. | 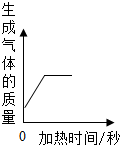 加热一定质量的高锰酸钾制取氧气 | |
| B. | 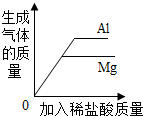 向等质量的铅粉和镁粉中分别滴入质量分数相同的足量的稀盐酸 | |
| C. | 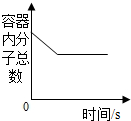 氢气和过量的氧气在密闭容器中完全反应 | |
| D. |  向一定质量的氯化铁和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液 |
分析 A、依据反应的化学方程式,分析反应条件与实际操作,然后与图象反映出的关系相比较,进行判断;
B、根据镁的活动性比铝强,镁与稀盐酸反应比铝剧烈,等质量两金属完全反应后,依据反应的化学方程式可知,铝产生氢气质量大于镁进行分析
C、根据氢气燃烧时分子的变化分析判断;
D、向盐酸和氯化铁的混合溶液中,逐滴加入氢氧化钠溶液,氢氧化钠会先和盐酸发生反应,待盐酸完全反应后,氢氧化钠才会和氯化铁发生反应形成氢氧化铁沉淀;
解答 解:A、反应的化学方程式为:2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,可见反应条件为加热,当加热到一定温度时该反应才能发生,故开始加热时无氧气产生,与图象不吻合,故A对;
B、根据题中的叙述可知,横坐标代表的是稀盐酸的质量,而不是反应时间,向等质量的铝粉和镁粉中分别滴入质量分数相同的足量的稀盐酸,所以对于酸来说刚开始滴加金属是过量的,Al和Mg产生的氢气一样多,随着反应的进行,活动性强的金属会先消耗完,然后另一种金属会继续反应,等质量的金属铝生成的氢气比镁生成的多,图象能正确反映对应操作,故B正确;
C、由氢气燃烧的方程式2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O可知,燃烧前后分子个数不断减少直到反应结束,分析与图象符合,故C错误.
D、向盐酸和氯化铁的混合溶液中,逐滴加入氢氧化钠溶液,氢氧化钠会先和盐酸发生反应,此时沉淀的质量为0,待盐酸完全反应后,氢氧化钠才会和氯化铁发生反应形成氢氧化铁沉淀,随着氢氧化钠溶液的加入,氯化铁完全反应,此时沉淀的质量不变.故D正确;
答案:A.
点评 在解此类题时,首先明确选项中叙述的反应原理,然后结合图象中的转折点进行分析解答.


科目:初中化学 来源: 题型:解答题
 冬季市场上热销一种叫“暖宝宝”取暖贴.取暖贴的持续放热可以促进人体微循环,恢复正常的生理机能,从而消除疼痛,治疗疾病.对关节炎、肩周炎、腰腿痛等病痛都有很好的效果的.右图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.
冬季市场上热销一种叫“暖宝宝”取暖贴.取暖贴的持续放热可以促进人体微循环,恢复正常的生理机能,从而消除疼痛,治疗疾病.对关节炎、肩周炎、腰腿痛等病痛都有很好的效果的.右图是某“取暖片”外包装的图片.该“取暖片”中发热剂主要成分有铁粉、活性炭、氯化钠、水等,其发热是利用铁生锈时会放热.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | Ca0 (CaCO3) | H2O | 过滤 |
| B | NaCl溶液(CaCl2) | 适量的Na2CO3溶液 | 过滤 |
| C | CO2 (H2O) | 固体氢氧化钠 | 洗气 |
| D | CuO(Cu) | 适量的稀盐酸 | 过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 钢铁被誉为现代工业的筋骨,是应用最广泛的金属材料.
钢铁被誉为现代工业的筋骨,是应用最广泛的金属材料.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某兴趣小组利用如图装罝(省略夹持仪器)探究二氧化碳与氢氧化钠溶液的反应
某兴趣小组利用如图装罝(省略夹持仪器)探究二氧化碳与氢氧化钠溶液的反应查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com