
【题目】化学与人类生活、生产活动息息相关。根据所学化学知识回答下列问题:
①自来水厂净水过程中除去色素和异味用到_____,其作用是吸附作用:
②家用天然气的主要成分是甲烷,写出甲烷燃烧的化学方程式_____;
③炒菜时,不小心将食盐洒落在火焰上,会发出_____颜色。
④复课后,学校每天会在教室喷撒二氧化氯(ClO2)溶液等消毒液,喷洒后,室内充满消毒液气味,这说明_____(从微观角度分析),ClO2由_____种元素组成,其中Cl元素的化合价为_____,1molClO2中约含_____个Cl原子。
【答案】活性炭 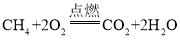 黄 分子不断运动 2 +4 6.02×1023
黄 分子不断运动 2 +4 6.02×1023
【解析】
①活性炭具有吸附性,可以吸附水中的色素和异味,故填:活性炭;
②甲烷燃烧生成二氧化碳和水,该反应的化学方程式为: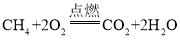 ;
;
③ 氯化钠中含钠离子,钠离子燃烧发出黄色火焰,故填:黄;
④分子是不断运动的,二氧化氯分子四处扩散,因此教室里充满消毒液气味,故填:分子不断运动;
ClO2由Cl、O两种元素组成,故填:2;
氧元素通常为-2价,设ClO2中氯元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:x+(-2)×2=0,x=+4;
1molClO2中约含:1mol×6.02×1023=6.02×1023个氯原子,故填:6.02×1023。


科目:初中化学 来源: 题型:
【题目】实验小组用pH传感器探究稀盐酸和氢氧化钠溶液的反应。实验操作和测定结果如图所示:

(1)盐酸和氢氧化钠反应的化学方程式为_____。
(2)该实验中,甲溶液是_____。
(3)能说明盐酸与氢氧化钠发生化学反应的依据是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验室里,同学们准备研究氢氧化钠能与二氧化碳反应的化学性质。
①在配制NaOH溶液时,看到盛有NaOH固体的试剂瓶上标注着“NaOH含量不少于96.0%”,便对该瓶试剂成分产生了质疑:
[提出问题]氢氧化钠中含有什么杂质?
[查阅资料]工业上制取NaOH的反应原理: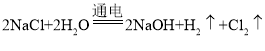 然后蒸发溶剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
然后蒸发溶剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
[提出猜想]
甲同学认为杂质只有氯化钠;
乙同学认为杂质还可能含有碳酸钠,原因为_______ (用化学方程式表示)。
[设计实验]取样溶于水,并分成两份。
步骤1:向一份溶液中滴加酚酞试液,溶液变_________色。
步骤2:向另一份溶液中滴加过量稀硝酸,有气泡产生。
步骤3:向步骤 2所得溶液中继续滴加_________溶液,发现有白色沉淀产生。
[实验结论]乙同学的猜想正确。
请
Ⅰ.上述实验中步骤_____(填序号)是没有必要进行的。
II.步骤2所得溶液中的溶质有________。
②同学们在配制好的氢氧化钠溶液中通入CO2气体,没有明显现象,于是设计了如下实验证明反应的发生:(不考虑氢氧化钠中的极少量杂质)
实验1 | 实验2 | 实验3 |
现象:烧杯中溶液几乎充满整个试管。 |
现象: 充分反应后,红墨水最终呈现左高右低现象。 |
现象: 滴加试剂X后,溶液中出现大量白色沉淀。 |
I .实验3中加入的试剂X是_______ (任写一种符合要求的试剂)。
II.实验1、2在设计思想上是一致的,都是通过验证反应物的消耗才能观察到明显现象,但有同学对实验1提出了质疑,他认为这个实验不足以证明CO2与NaOH发生了化学反应,其理由是_______。
Ⅲ.查阅资料:室温下,氢氧化钠易溶于酒精,而碳酸钠难溶于酒精。据此,同学们设计了实验4,请你补充完整。
实验4步骤 | 实验现象 | 实验结论 | 实验分析 |
将CO2气体不断地通入氢氧化钠酒精溶液中,观察现象。 | _______ | 氢氧化钠与二氧化碳确实发生了化学反应。 | 实验4与实验____(填实验序号)的设计思想是一致的,都是根据生成物的性质才能观察到明显现象。 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b、c三种物质的溶解度曲线如下图。t1℃时,现取a、b、c三种物质各20g加入到100g水中,充分溶解后,得到a、b、c三种物质的混合物。下列说法正确的是( )
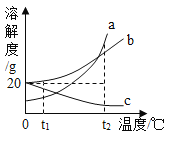
A.t1℃时,a溶液中的溶质质量分数最大
B.将其都升温至t2℃时,c溶液中的溶质质量分数最小
C.t1℃时,a、b溶液均为不饱和溶液
D.将其都升温至t2℃时,a、b溶液中溶质的质量分数变大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】西西和建设两位同学为探究硫酸的化学性质,做了如下实验:
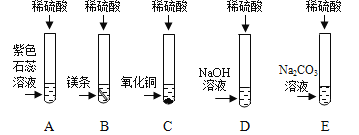
试管 A 中的现象是___________,反应后试管 B 中可能含有的离子是______________(写离子符号);试管 C 中反应的化学方程式__________;建设同学把 D、E 试管内反应后的溶液倒入同一个烧杯中,观察到无明显现象,建设同学认为 D 试管中氢氧化钠溶液和稀硫酸一定恰好完全反应,请评价建设同学的说法___________。
(提出问题)E 试管中反应后溶液中溶质是什么?
猜想一:Na2SO4
猜想二:Na2SO4、H2SO4
西西同学的猜想:_____________(写化学式)
(实验验证)西西同学取少量 E 试管反应后液体于试管中,向其中加入_____________观察到_____________,证明自己的猜想是正确的。结合建设同学的实验,可推知 D 试管溶液中溶质为______________。
(交流总结)在分析某溶液含有的溶质时,可根据与其混合的溶液中(9) ____________及混合后的___________来得出结论。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】①地壳中含量第2高的金属元素_____
②1个钙离子_____
③丙酮(![]() )是一种重要的石油化工产品,它属于_____(有机物,无机物)
)是一种重要的石油化工产品,它属于_____(有机物,无机物)
④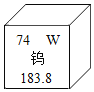 周期表中钨元素的信息如图所示,它属于_____号元素,判断钨的相对原子质量是_____
周期表中钨元素的信息如图所示,它属于_____号元素,判断钨的相对原子质量是_____
⑤比较铜和铁的熔点,哪个更大_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】认识物质及其变化,对于了解自然现象和规律至关重要。
(1)下列是初中化学常见的实验或操作,回答下列问题:
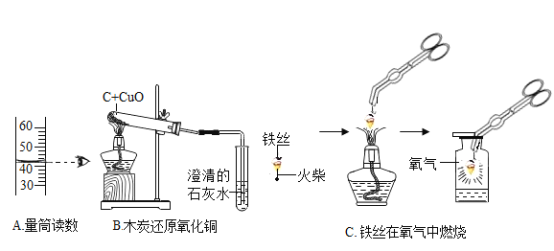
①A实验中读出液体的体积为_____mL。
②B实验中观察到的实验现象是_____。
③C实验集气瓶内预先装入少量的水的目的是_____,铁丝燃烧的化学方程式为_____。
(2)在烧杯中加入5.74g久置于空气中的铝箔,再滴加稀硫酸,放出气体的质量与所加稀硫酸质量的关系如图所示。请回答下列问题:
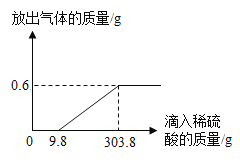
①产生氢气(H2)的总质量为_____;
②刚滴加稀硫酸时无氢气放出,是因为稀硫酸与铝箔表面的物质_____(填化学式)反应,该物质与稀硫酸反应的化学方程式为_____。
③请计算铝箔中含有金属铝的质量_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属在生产、生活中有着广泛的应用。
(1)保护金属资源的有效途径之一是防止金属锈蚀。自行车的链条常采用的防锈方法是___________。铁制品一旦生锈,可用稀硫酸除铁锈,请写出相应的化学方程式___________。
(2)铁是年产量最高的金属,工业上用赤铁矿(主要成分是氧化铁)炼铁的化学反应原理用化学方程式表示为___________。
(3)将一定质量的锌粉和铁粉放入硝酸镁和硝酸银的混合溶液中,充分反应后过滤所得滤液中一定含有的阳离子___________(写离子符号),向滤渣中加入稀盐酸,如果有气泡产生,滤渣中一定有___________(写化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分析以下化学反应的微观示意图,判断有关说法正确的是( )
A. 反应前后各物质均属于氧化物
B. 参加反应的两种物质的分子个数比为2:3
C. 该反应中各元素的化合价均发生了改变
D. 在化学反应中,分子可以再分,原子不可再分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com