
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:初中化学 来源: 题型:
| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
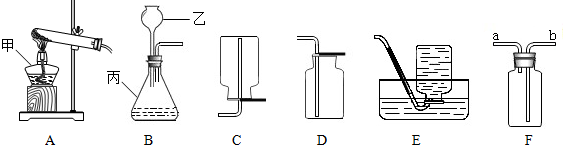
 (2011?北京)右图装置可以完成多个简单实验,具有药品用量少、实验现象明显、尾气不外逸等优点.
(2011?北京)右图装置可以完成多个简单实验,具有药品用量少、实验现象明显、尾气不外逸等优点.| 滴管甲 | 烧杯① | 滴管乙 | 烧杯② | |
| 试剂 | H2O | NaOH(或浓硫酸或生石灰). NaOH(或浓硫酸或生石灰). |
稀盐酸 稀盐酸 |
Mg |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
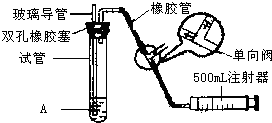 二氧化硫是大气污染物之一,为粗略地测定周围环境中的SO2含量,某学生课外活动小组设计了如图的实验装置.
二氧化硫是大气污染物之一,为粗略地测定周围环境中的SO2含量,某学生课外活动小组设计了如图的实验装置.| S02最高浓度限值(单位mg?m-3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
| 分组 | 第一小组 | 第二小组 |
| 抽气次数 | 120 | 140 |
| 空气中S02的含量(单位:mg?m-3) |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
| 除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的氯化钙溶液, 充分反应后过滤 |
白色沉淀 白色沉淀 |
有关反应的化学方程式为 Na2CO3+CaCl2=2NaCl+CaCO3↓ Na2CO3+CaCl2=2NaCl+CaCO3↓ |
| 检验是否含有氢氧化钠 | 向过滤后的滤液中滴入 酚酞试液 酚酞试液 |
变红 变红 |
该样品中含有氢氧化钠 |
| 106 |
| x |
| 44 |
| 4.4g |
| 10.6g |
| 16.40g |
| 106 |
| x |
| 44 |
| 4.4g |
| 10.6g |
| 16.40g |
| 加入盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | 第七次 |
| 锥形瓶及所盛物质的总质量 | 76.40 | 101.40 | 126.40 | 151.40 | 174.20 | 197.00 | 222.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com