
| A. |  CO2验满 | B. | 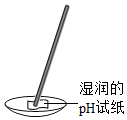 测溶液酸碱度 | C. | 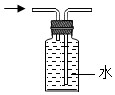 收集O2 | D. | 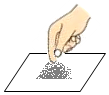 取用固体药品 |
分析 A、根据二氧化碳气体的验满方法进行分析判断.
B、根据用pH试纸测定未知溶液的pH的方法进行分析判断.
C、根据图中装置用排水法收集气体时,长导管是出水管,进行分析判断.
D、根据固体药品的取用方法进行分析判断.
解答 解:A、检验二氧化碳是否收集满时,应将燃着的木条放在集气瓶口,不能伸入瓶中,图中所示操作错误.
B、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,不能用水湿润pH试纸,否则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确,图中所示操作错误.
C、氧气不易溶于水,用图中装置收集氧气时,长导管是出水管,短导管是进气管,图中所示装置正确.
D、取用固体粉末状药品时,应用药匙取用,不能用手接触药品,图中所示操作错误.
故选:C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | “反应”步骤中Cl的化合价不变 | |
| B. | 回收得到的NaHSO4 属于酸 | |
| C. | “电解”步骤中的主要反应方程式为:2ClO2+2NaCl=2NaClO2+Cl2,该反应属于置换反应 | |
| D. | “尾气吸收”是吸收“电解”过程排出的少量ClO2,这样做的目的是提高原料的利用率 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
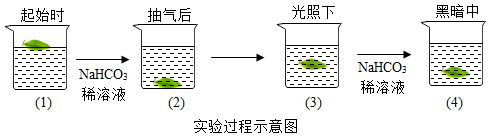
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某班同学实验后收集到含有碳酸钠和氢氧化钠的混合废液5.11Kg,一个兴趣小组用废弃的溶质质量分数为19.6%的硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求:
我们知道,每次做完实验后,剩余废液不能直接倾倒入排污管,必须回收处理.某班同学实验后收集到含有碳酸钠和氢氧化钠的混合废液5.11Kg,一个兴趣小组用废弃的溶质质量分数为19.6%的硫酸来处理,并回收处理后的溶液.他们向废液中加入稀硫酸时,所得溶液pH与加入的稀硫酸质量的关系曲线如图所示.求:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com