
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO还原Fe2O3的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | |
| B. | 原子是由原子核和中子构成的 | |
| C. | 五氧化二磷的化学式为P2O5 | |
| D. | 小孩发烧时,医生经常会用酒精给小孩擦身体,这是因为酒精汽化吸热 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
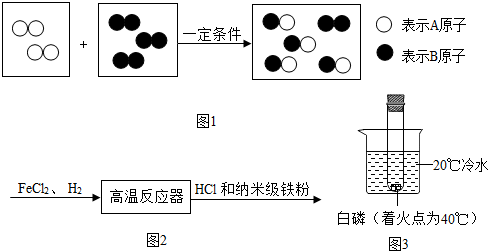
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
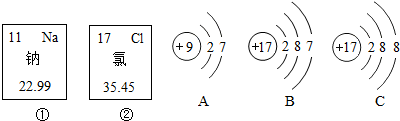
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 置换反应有单质生成,则有单质生成的反应一定为置换反应 | |
| B. | 实验室中,点燃H2前需要验纯,则点燃其它可燃性气体前也需要验纯 | |
| C. | KNO3的溶解度随温度的升高而增大,则其它物质的溶解度均会随温度的升高而增大 | |
| D. | 单质中只含一种元素,则只含一种元素的物质一定是单质 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 四种物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 25 | 15 | 1 | 5 |
| 反应后质量(g) | 11 | 未测值 | 1 | 22 |
| A. | 未测值为3g | B. | 丙可能是催化剂 | ||
| C. | 甲与乙反应的质量比为3:14 | D. | 该反应可能是分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
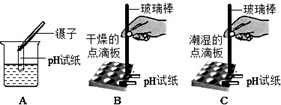
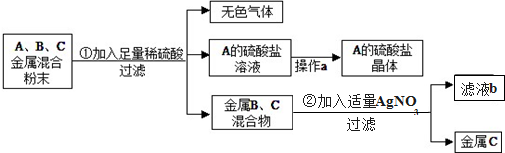
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com