
分析 根据碳酸钡沉淀难溶于水,硝酸铜和氢氧化钠会生成氢氧化铜沉淀,碳酸钡和盐酸反应会生成二氧化碳,氢氧化铜沉淀和盐酸反应会生成蓝色的氯化铜溶液,硫酸根离子和钡离子会生成硫酸钡沉淀,氯离子和银离子会生成氯化银沉淀等知识进行分析.
解答 解:碳酸钡沉淀难溶于水,硝酸铜和氢氧化钠会生成氢氧化铜沉淀,碳酸钡和盐酸反应会生成二氧化碳,氢氧化铜沉淀和盐酸反应会生成蓝色的氯化铜溶液,硫酸根离子和钡离子会生成硫酸钡沉淀,氯离子和银离子会生成氯化银沉淀.
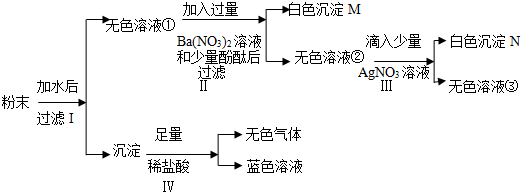
粉末加水溶解后,得到沉淀和无色溶液,沉淀中加入盐酸会生成无色气体和蓝色溶液,所以蓝色溶液是氯化铜溶液,沉淀中含有氢氧化铜沉淀,无色粉末中一定含有硝酸铜和氢氧化钠,碳酸钡和盐酸会生成二氧化碳气体,所以粉末中一定含有碳酸钡,无色溶液中加过量的硝酸钡溶液和酚酞,生成白色沉淀M和无色溶液,所以无色溶液中不含氢氧化钠,生成白色沉淀M证明一定含有硫酸钠,无色溶液中加硝酸银会生成白色沉淀N,所以白色沉淀N是氯化银沉淀,粉末中一定含有氯化钠,所以,
(1)通过推导可知,沉淀M是硫酸钡沉淀,化学式为:BaSO4;故填:BaSO4;
(2)步骤Ⅳ中有气体生成的反应是碳酸钡和盐酸反应生成氯化钡、水和二氧化碳,故化学方程式为:BaCO3+2HCl═BaCl2+H2O+CO2↑;
(3)无色溶液②和硝酸银会生成氯化银沉淀,所以无色溶液②中含有氯化钠,过量的硝酸钡和硫酸钠反应生成硫酸钡沉淀和硝酸钠,所以溶液②中含有硝酸钡、硝酸钠,所以无色溶液②中一定存在的溶质(酚酞除外)的化学式:NaNO3、Ba(NO3)2、NaCl;故填:NaNO3、Ba(NO3)2、NaCl;
(4)通过推导可知,这包粉末中含有氯化钠、碳酸钡、硝酸铜、硫酸钠、氢氧化钠五种物质;故填:五.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.


科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量反应后的溶液于试管中,滴加酚酞试液 | 溶液不变红色 | 理想Ⅲ不正确 |
| ②再另取少量反应后的溶液于另一支试管中,向里面加入适量CaCO3 | 有气泡生成 | 猜想Ⅰ不正确 猜想Ⅱ正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 空气的成分按体积计算,氧气约占21% | |
| B. | 干冰可作制冷剂 | |
| C. | 食品包装中充入氮气防腐 | |
| D. | 将带火星的木条伸入氧气集气瓶中,木条复燃,证明氧气已收集满 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 投入几小块烘烤过的木炭.红棕色会消失的原因是木炭有吸附性,吸附NO2,红棕色消失;
投入几小块烘烤过的木炭.红棕色会消失的原因是木炭有吸附性,吸附NO2,红棕色消失; 装置中玻璃管的作用是引燃红磷、使瓶内气体进入气球中;
装置中玻璃管的作用是引燃红磷、使瓶内气体进入气球中;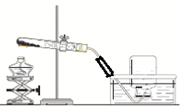 根据质量守恒定律解释高锰酸钾受热分解后,剩余固体的质量比原反应物的质量小的原因高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,反应后氧气逸出,故剩余固体的质量比原反应物的质量小.
根据质量守恒定律解释高锰酸钾受热分解后,剩余固体的质量比原反应物的质量小的原因高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,反应后氧气逸出,故剩余固体的质量比原反应物的质量小.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | ①②③⑤⑥ | B. | ③④⑤⑥⑦ | C. | ①②⑤⑥⑦ | D. | ①②③④⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
| 名称 | 洗涤灵 | 洁厕灵 | 炉具清洁剂 | 活氧彩漂 | 污渍爆炸盐 |
| 产品样式 |  |  |  |  |  |
| 有效成分或功能 | 清洗油污 | 盐酸 | 氢氧化钠 | 过氧化氢 | 过碳酸钠 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com