

���� ������101.2g��CaCl2��HCl����Һ����μ���������������Ϊ10%��Na2CO3��Һʱ��̼�����Ⱥ�ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼�����ﵽa��ʱ��̼���ƺ�ϡ������ȫ��Ӧ������2.2g������̼��̼�����ٺ��Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ�����̼��Ƶ�������5.0g���Ȼ�����Һ�����ԣ�pH=7��ϡ���������ԣ�pH��7���з�����
��� �⣺��1��db�εķ�Ӧ��̼���ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼����ѧ����ʽΪ��Na2CO3+2HCl�T2NaCl+H2O+CO2����K���ʾ�������ǣ�̼�������Ȼ��ơ�ϡ������ȫ��Ӧ��
��2����b��ʱ����̼���Ƶ�����Ϊx�������Ȼ��Ƶ�����Ϊy��
Na2CO3+2HCl�T2NaCl+H2O+CO2����
106 117 44
x y 2.2g
$\frac{106}{x}$=$\frac{117}{y}$=$\frac{44}{2.2g}$
x=5.3g
y=5.85g
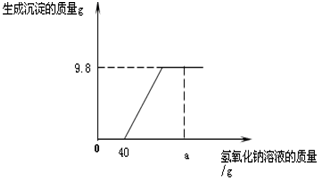
ͼ1��b������̼������Һ������Ϊ��$\frac{5.3g}{10%}$=53g��
�����Ȼ��Ʒ�Ӧ��̼���Ƶ�����Ϊm�������Ȼ��Ƶ�����Ϊn
Na2CO3+CaCl2�TCaCO3��+2NaCl��
106 100 117
m 5.0g n
$\frac{106}{m}$=$\frac{100}{5g}$=$\frac{117}{n}$
m=5.3g
n=5.85g
���Բμӷ�Ӧ��̼������Һ����Ϊ��$\frac{5.3g}{10%}$=53g������x=106g��
aʱ��Һ�е��������Ȼ��ơ��Ȼ��ƣ�c��ʱ��Һ�е��������Ȼ��ƣ�
��3����Һ����Ϊ��101.2g+53g+53g-2.2g-5.0g=200g��
��Һ�е�������������Ϊ��$\frac{5.85g��2}{200g}$��100%=5.85%��
�ʴ�Ϊ����1��Na2CO3+2HCl�T2NaCl+H2O+CO2����̼�������Ȼ��ơ�ϡ������ȫ��Ӧ��
��2��53g��106g���Ȼ��ơ��Ȼ��ƣ��Ȼ��ƣ�
��3��5.85%��
���� ������Ҫ�����˻�ѧ����ʽ�ļ��㣬�ѶȽϴ���Ҫ���������Ӧԭ����Ȼ���������е����ݼ�С���㣬ע������ȷ�Ժ淶�ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���нֵ���ˮ���� | B�� | ¶����սոѡ���Ҷ | ||
| C�� | ��չˮ������������ | D�� | ��Ǩ���ظ��Ƿ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 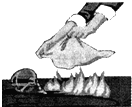 �ƾ���ʧ����ʪ���̸� | B�� | 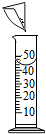 ��NaCl������Ͳ��������Һ | ||
| C�� |  �Ӽ���ĥ������ζ�����̬���� | D�� | 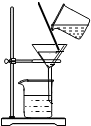 ������Һ��������KNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | ����ϡ���������/g | ʣ����������/g |
| 1 | 20 | 15 |
| 2 | 20 | 10 |
| 3 | 20 | 6.8 |
| 4 | 20 | n |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
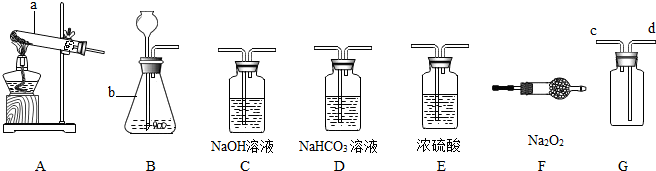
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com