
| ���ձ� | ��������� | ����Ͻ�� 5���� | ����Ͻ�� 12���� | ����Ͻ�� 21���� | ����Ͻ�� 40���� | ����Ͻ�� 3Сʱ | |
| ������g�� | 28.5 | 169.7 | 183.6 | 183.5 | 183.4 | 183.3 | 183.3 |
���� ���ݱ����ṩ��������������������������ٸ��ݻ�ѧ����ʽ�������������ط��������
��� �⣺��1����Ϊ�����Ũ��Խ��ӦԽ�죬���ŷ�Ӧ�Ľ��У������Ũ�ȼ�С����Ӧ�ٶȱ��������������������ٶ��ɿ������
��2���⣺��Ͻ���Fe������Ϊx�����ɵ�FeSO4����Ϊy��
����������������169.7g+14.0g-183.3g=0.4g��
Fe+H2SO4=FeSO4+H2��
56 152 2
x y 0.4g
$\frac{56}{x}=\frac{152}{y}=\frac{2}{0.4g}$
x=11.2g��y=30.4g��
��Һ������Ϊ��11.2g+��169.7g-28.5g��-0.4g=152.0g��
��������������������$\frac{30.4g}{152.0g}$��100%=20%��
��������������������Ϊ20%��
��3���Ͻ�����Ԫ�ص���������Ϊ��$\frac{11.2g}{14.0g}$��100%=80%��
�𣺺Ͻ�����Ԫ�ص���������Ϊ80%��
���� ���ݱ����ṩ����Ϣ�����жϷ�Ӧ���е��������������ƽ�������ٱ仯ʱ��˵���Ѿ���ȫ��Ӧ������������������������������������һ�����������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ƣ�OCa�� | B�� | ����þ��MgO2�� | C�� | ������������Fe3O2�� | D�� | �Ȼ�����BaCl2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu+FeS04�TFe+CuS04 | B�� | Zn+2AgNO3�T2Ag+Zn��NO3��2 | ||
| C�� | 2Al+CuS04�TCu+Al2S04 | D�� | 2Fe+3CuCl2�T2FeCl3+3Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��ij��������ˮ��ų�������˵���ù�����һ�������������� | |
| B�� | ����ɫ����ͭ��ĩ¶���ڿ����б���ɫ��˵�������к���ˮ���� | |
| C�� | ���Ȼ�����Һ�μӵ�ij��Һ�г��ְ�ɫ������˵������Һ�п��ܺ������������ | |
| D�� | ��������ձ���������Ļ����Ϸ����ڱڳ���Сˮ�飬˵�������к�����Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
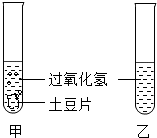 С����һƬ�����������������Һ�У����ֹ���������Һ�ķֽ����ʼӿ죮�������Ϻ�֪�������к���һ���������--��������ø�����������������ʵ�飺�����½���Ƭ����������Թܣ��ֱ����ס����Թ���ע����ͬ������������������Ĺ���������Һ����ͼ��ʾ�����۲��Թ������ݲ��������ʣ�
С����һƬ�����������������Һ�У����ֹ���������Һ�ķֽ����ʼӿ죮�������Ϻ�֪�������к���һ���������--��������ø�����������������ʵ�飺�����½���Ƭ����������Թܣ��ֱ����ס����Թ���ע����ͬ������������������Ĺ���������Һ����ͼ��ʾ�����۲��Թ������ݲ��������ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
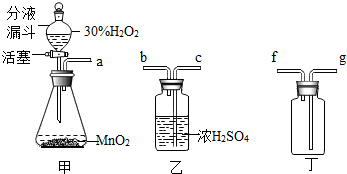 ��֪2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����ʵ���������ø÷�Ӧ��ѡ����ͼ��ʾװ�ÿ���ȡ��������ش��������⣺
��֪2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2����ʵ���������ø÷�Ӧ��ѡ����ͼ��ʾװ�ÿ���ȡ��������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
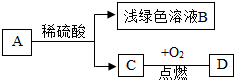 ��֪��A��B��C��D��������֮���������ת����ϵ������C�ǵ��ʣ�D����Է���������С��������Իش�
��֪��A��B��C��D��������֮���������ת����ϵ������C�ǵ��ʣ�D����Է���������С��������Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ��Ŀ�� | ʵ�鲽�� | ʵ�������� |
| ̽�����ֽ����������������Ӧ�ж����������� | �����Թ��м�����һ��Ũ�ȹ���������Һ���Ժ�����ľ�������Թܣ� �������Թ��м��������������̣���������ľ�������Թܣ� �����Թ���������ʱ�����¼�H2O2Һ����������ľ�������Թܣ����ظ��������� | ľ������ȼ�����������٣� �������ݣ�ľ����ȼ�����������ࣻ ľ����ȼ���������̵����ޱ仯����Ӧ��������ã� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com