
 兴趣小组同学对“氢氧化钠溶液与硫酸混合是否发生发应”进行了如下探究:
兴趣小组同学对“氢氧化钠溶液与硫酸混合是否发生发应”进行了如下探究:| 实验操作 | 实验现象 | |
| 甲同学 | 在盛有10mL一定浓度的氢氧化钠溶液的烧杯中,用胶头滴管慢慢滴入硫酸,不断振荡溶液,同时测定溶液的pH. | 溶液pH不断减小,最终小于7. |
| 乙同学 | 在盛有10mL一定浓度的氢氧化钠溶液的烧杯中,先滴入几滴无色酚酞试液,然后再加入硫酸并不断搅拌. | 溶液由红色变为无色. |
分析 【设计并实验】根据溶液酸碱性与无色酚酞试液的变色情况分析;
(1)根据氢氧化钠与稀硫酸反应写化学方程式;
(3)根据图示判断;
(4)根据氢氧化钠与稀硫酸反应后氢氧化钠会消失,来设计对比实验;
解答 解:【设计并实验】无色酚酞试液遇碱变红,遇中性或酸性物质不变色;
(1)氢氧化钠与稀硫酸反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O;
(3)根据图示分析,硫酸和氢氧化钠的反应是放热反应,当加入稀硫酸10mL时,二者恰好完全反应.
(4)实验方案为:取两支试管各加入10mL10%的氢氧化钠溶液,分别向两只试管中加入10mL蒸馏水和上述浓度的稀硫酸,再分别加入硫酸铜溶液,前者有蓝色沉淀产生,后者无明显现象,即证明二者混合发生了反应.
故答案为:
【设计并实验】红;无
(1)2NaOH+H2SO4═Na2SO4+2H2O;
(3)放热;10;
(4)取两支试管各加入10mL10%的氢氧化钠溶液,分别向两只试管中加入10mL蒸馏水和上述浓度的稀硫酸,再分别加入硫酸铜溶液,前者有蓝色沉淀产生,后者无明显现象,即证明二者混合发生了反应.
点评 本题较综合的考查了学生对酸和碱化学知识的掌握和应用,掌握并理解知识才能熟练地利用知识设计实验、分析解决相关问题.


科目:初中化学 来源: 题型:选择题
| A. | 用稀硫酸除去铁锈:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O 复分解反应 | |
| B. | 电解水时,两极均产生气泡:2H2O $\frac{\underline{\;电解\;}}{\;}$2H2+O2↑ 分解反应 | |
| C. | 实验室制取二氧化碳:CaCO3+HCl═CaCl2+H2O+CO2↑ 中和反应 | |
| D. | 用磁铁矿炼铁:4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
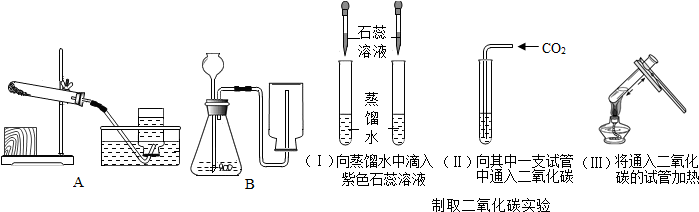
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 现象 | 结论 |
| ①将足量铁粉与锌粉分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率:Fe<Zn | 反应速率与反应物的金属活动性强弱有关 |
| ②将等质量锌粉与锌片分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率:锌粉>锌片 | 反应速率与反应物的接触面积大小有关 |
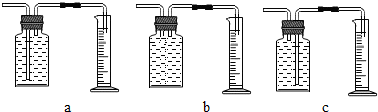
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 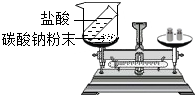 验证质量守恒定律 | B. | 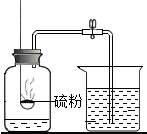 测定空气中的氧气含量 | ||
| C. |  证明CO2密度比空气大 | D. |  证明CO2能与水反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com