
 氢氧化钙溶液俗称熟石灰,在生产和生活中有广泛的用途.请根据所学化学知识回答下列问题:
氢氧化钙溶液俗称熟石灰,在生产和生活中有广泛的用途.请根据所学化学知识回答下列问题:分析 (1)根据化合价代数和为零进行分析;
根据氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水进行分析;
(2)①根据碳酸钾和氢氧化钙反应生成碳酸钙沉淀和氢氧化钾进行分析;
②根据植物需要的营养元素有N、P、K,“黑白粉”中含有K元素进行分析;
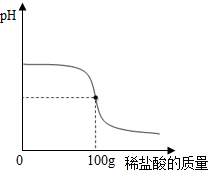
③根据氢氧化钾和盐酸反应生成氯化钾和水,依据题中的数据进行计算.
解答 解:(1)Ca(OH)2中氢氧根离子显示-1价,所以钙元素的化合价为+2,用熟石灰配成的石灰浆可以粉刷墙壁.干燥后墙面会变硬,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,这时白色墙面的主要成分是碳酸钙,故选:D;
(2)①碳酸钾和氢氧化钙反应生成碳酸钙沉淀和氢氧化钾,化学方程式为:Ca(OH)2+K2CO3=CaCO3↓+2KOH;
②植物需要的营养元素有N、P、K,“黑白粉”中含有K元素;
③设所得溶液中溶质的质量为x
KOH+HCl=KCl+H2O
36.5 74.5
14.6%×100g x
$\frac{36.5}{14.6%×100g}$=$\frac{74.5}{x}$
x=29.8g
故答案为:(1)+2,D;
(2)①Ca(OH)2+K2CO3=CaCO3↓+2KOH;
②K;
③29.8g.
点评 本题主要考查化学方程式的计算,难度不大,注意解题的规范性和准确性.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 它们的最主要区别是:分子可再分而原子不可再分 | |
| B. | 分子是由原子构成的 | |
| C. | 原子是化学变化中最小的粒子 | |
| D. | 分子、原子都是构成物质的基本粒子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 物质的三态变化--分子的间隔发生了改变 | |
| B. | 端午时节粽飘香--分子在不断的运动 | |
| C. | 过氧化氢分解制氧气--分子在化学变化中可以再分 | |
| D. | 金刚石和石墨物理性质差异大--碳原子的结构不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com