
在生产生活中,你会发现“化学就在身边”。
(1)洗洁精能清除油污,这是利用它的________作用。
(2)上海世博园内安装的“直饮水”机,采用“活性炭+超滤层+紫外线”净水工艺。活性炭在此起_________作用,净化后的水属于________(选填
 “混合物”或“纯净物”)。
“混合物”或“纯净物”)。
(3)在农业生产中,施用的草木灰(有效成份为K2CO3)属于_______肥。在含有硫酸镁、硫酸铜的工业废水中加入过量的锌粉,充分反应后过滤,所得固体是(填写化学式)___________。
(4)化学对体育不仅雪中送炭,而且锦上添花。举重、体操等项目的运动员在比赛前常用白色的“镁粉”搓手,这是因为“镁粉”质轻、吸水性好,可做防滑剂。 “镁粉”的有效成份是碱式碳酸镁,它不可燃,300℃即分解,其分解的化学方程式是:
Mg5(OH)2(CO3)4 △ 5MgO+X+4CO2↑,则X的化学式是________;根据这些信息,还能推断出“镁粉”的另一种用途是________。
科目:初中化学 来源: 题型:
下列有关金属的说法错误的是( )
A.常温下金属均为固态
B.合金的很多性能与组成它们的纯金属不同
C.铁在潮湿的空气中比在干燥的空气中更易生锈
D.铝在空气中表面会生成致密的氧化铝薄膜,使铝具有很好的抗腐蚀性能
查看答案和解析>>
科目:初中化学 来源: 题型:
下列有关铁的说法不正确的是( )
A.生铁和钢都是铁合金
B.铁是地壳中含量最多的金属元素
C.工业炼铁的原理是:3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
D.用铁制作铁锅利用了铁的导热性
查看答案和解析>>
科目:初中化学 来源: 题型:
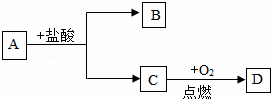
已知,A,B,C,D四种物质之间存在以下转化关系,其中AC是单质,D是相对分子质量最小的氧化物,B为浅绿色溶液,试回答.
(1)写出A,C,D三种物质的化学式:
A. ,C. ,D. ;
(2)请你写出A→B+C的化学方程式 .
查看答案和解析>>
科目:初中化学 来源: 题型:
精还原铁粉是一种重要的化工原料,某兴趣小组对其进行下列研究:
【物质制备】利用绿矾制备精还原铁粉的工艺流程如下:
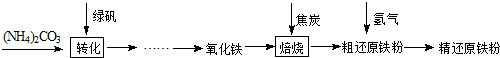
FexOy+yH2 xFe+yH2O Fe3C+2H2
xFe+yH2O Fe3C+2H2 3Fe+CH4粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为: .
3Fe+CH4粗还原铁粉中还含有少量铁的氧化物和Fe3C杂质,可用氢气在高温下进一步还原,其反应方程式为: .
(1)写出焙烧中氧化铁与CO反应的化学方程式 .
(2)焙烧中加焦炭的作用除了可以作燃料提供反应所需高温外,还能 .
【含量测定】甲同学为得到精还原铁粉并测定粗还原铁粉中氧和碳元素的质量分数,按如下装置进行实验.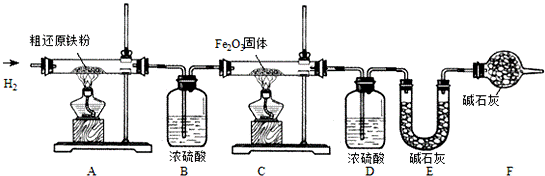
已知:3CH4+4Fe2O3 3CO2+6H2O+8Fe,浓硫酸有吸水性,碱石灰不仅能吸收水而且能吸收CO2.(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响).
3CO2+6H2O+8Fe,浓硫酸有吸水性,碱石灰不仅能吸收水而且能吸收CO2.(假设每步反应都完全且不考虑装置内原有空气对测定结果的影响).
(3)主要实验步骤如下:
①按顺序组装仪器,检查装置的气密性,称量样品和必要装置的质量;
②缓缓通入纯净干燥的H2;
③点燃C处酒精灯;
④点燃A 处酒精灯;
⑤分别熄灭A、C处酒精灯;
⑥ ;
⑦再次称量必要装置的质量.
(4)步骤②的目的是 ,验证该步骤目的达到的实验方法是 .
(5)反应后C装置中的现象是 .
(6)装置F的作用是 .
(7)若缺少装置D,则所测氧元素的质量分数将 (“偏大”、“偏小”或“不变”).
(8)实验后,甲同学根据装置 (填A、B、C、D、E、F)的增重分别算得样品中氧和碳元素的质量分数.
(9)乙同学将10.0克粗还原铁粉样品与足量稀盐酸充分反应,经测定共产生0.3克气体.计算该粗还原铁粉样品中铁单质的质量分数.(要求写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
现有Cu和CuO的固体混合物20g,为了分析混合物中Cu和CuO的含量,小冰同学利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究.
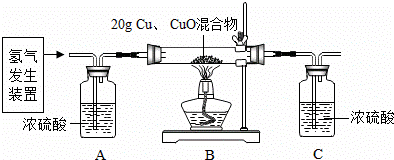
根据实验设计及有关数据进行分析与计算:
| 装置 | B | C |
| 反应前质量 | 85.3g | 284.2g |
| 反应后质量 | 82.1g | 287.8g |
(1)生成水的质量是 g.
(2)混合物中CuO的质量分数是为多少?(写出计算过程)
(3)该实验还可测定组成水的各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为 (不用化简);
若玻璃管中的氧化铜没有完全反应,则求得水中氢、氧元素的质量比会 (选填“偏大”、“偏小”或“不变”).
查看答案和解析>>
科目:初中化学 来源: 题型:
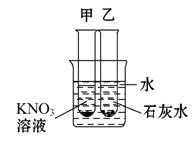
如图所示,在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),若使甲试管中晶体减少,乙试管中晶体增加,需向烧杯中加入的物质是
( )
A.氯化钠 B.氢氧化钠
C.冰块 D.硝酸钾
查看答案和解析>>
科目:初中化学 来源: 题型:
溶解度可表示物质溶解性的大小。
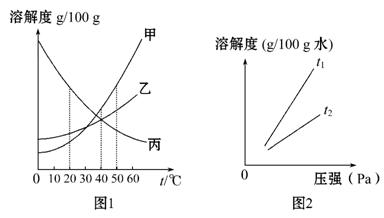
(1)如图1是甲、乙、丙三种固体 物质(均不含结晶水)的溶解度曲线。
物质(均不含结晶水)的溶解度曲线。
Ⅰ.40℃时,乙和丙 (填“能”或“不能”)形成溶质质量分数相同的饱和溶液。
Ⅱ.20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃。请填表:
| 烧杯中的溶质 | 烧杯中固体的变化 |
| 甲 | |
| 乙 | 固体逐渐减少至全部溶解 |
| 丙 |
(2)Ⅰ.打开可乐瓶,逸出大量气体,由此可见,压强越小,CO2的溶解度越 ,若要加大二氧化碳溶解的量可采用的一种方法是 _______。
Ⅱ.不同温度下,氧气的溶解度随压强的变化如图2所示,图中t1对应的温度为40℃,则t2对应的温度 (填序号)。
a.大于40℃ b.小于40℃ c.无法确定
查看答案和解析>>
科目:初中化学 来源: 题型:
(1)蜡烛在空气中燃烧时生成二氧化碳和水。由此判断蜡烛中一定含有的元素是 (填元素符号)。
(2)“84”消毒液可用于灾区防疫,其主要成分是次氯酸钠(NaClO),制取它的化学方程式为2NaOH+X═NaClO+NaCl+H2O,则X的化学式为 .求出NaClO中氯元素化合价并在该化学式中表示出来 。
(3)在反应A+3B=2C+2D中,14克A完全反应生成44克C和18克D,若A的相对分子质量为28,则B的相对分子质量是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com