
【题目】(8分)电石是一种重要的化工原料,极易与水反应:CaC2+2H2O=Ca(OH)2+X↑。
(1)将电石长期露置于空气中,会发生下列变化:
![]()
题干中电石与水反应后所得的气体X的化学式是_______,残渣中的主要成分是Ca(OH)2和_______ (写名称)。
(2)工业上利用电石制备某化工原料的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):
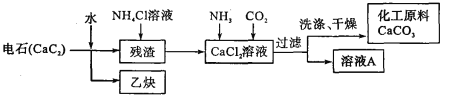
①CaCl2溶液中通人NH3、CO2两种气体,生成CaCO3的化学方程式为_______ 。
②流程中溶液A可循环使用,溶液A中的主要成分的化学式是_______。
③实验室中对过滤所得的固体进行洗涤在_______ 中进行,加洗涤剂时以浸没固体的量为宜。
(3)检验沉淀洗涤干净的方法:取最后一次洗涤液少量置于试管中滴加试剂硝酸银溶液,若观察到_______ ,则证明洗涤干净。
(4)电石应该_______保存。
【答案】(1)C2H2 碳酸钙
(2)①CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl ②NH4Cl ③过滤器
(3)无明显现象或无白色沉淀 (4)密封
【解析】
试题分析:(1)根据质量守恒定律的微观解释:在化学反应前后,原子的种类、数目都不变,结合化学反应:CaC2+2H2O=Ca(OH)2+X↑,可以推出X的化学式为C2H2;因为氢氧化钙会与空气的二氧化碳反应生成碳酸钙,故残渣中的主要成分是Ca(OH)2和 碳酸钙
(2)①CaCl2溶液中通人NH3、CO2两种气体,生成CaCO3的化学方程式为:CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl
②可循环使用的物质应是某个化学反应的生成物,又是某个化学反应的反应物,故流程中溶液A可循环使用,溶液A中的主要成分的化学式是NH4Cl
③实验室中对过滤所得的固体进行洗涤在过滤器中进行,加洗涤剂时以浸没固体的量为宜
(3)因为过滤所得的碳酸钙固体上可以粘有NH4Cl,故检验沉淀洗涤干净,实际就是检验洗涤液中是否含有NH4Cl,故方法为::取最后一次洗涤液少量置于试管中滴加试剂硝酸银溶液,若观察到无明显现象或无白色沉淀,则证明洗涤干净
(4) 根据上面的探究,电石应该密封保存


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:初中化学 来源: 题型:
【题目】(1)化学与生活密切相关,在厨房里蕴藏着许多化学知识。
①下列食物中,维生素含量比较丰富的是 (填字母序号);

②食盐是重要的调味品,食盐适量加碘可以有效预防碘缺乏引起的 。
③下列物品所用的材料中属于有机合成材料的是(填选项字母) 。
A、铝制高压锅 B、矿泉水瓶 C、玻璃杯
(2)南京市青奥会举行期间,为了控制汽车尾气给空气造成的污染,南京市在燃料的使用和管理等方面采取了一些有效措施,使用节能环保车也是未来的发展趋势。

①图1中公交车使用的天然气,其完全燃烧的化学方程式为 。
②图2是上海国际汽车展中,我国自行研制的氢动力概念跑车。汽车最理想的清洁燃料是氢气,氢气在空气中燃烧的化学方程式为 。
③图3是由上汽集团自主研发的“叶子”概念车,该车顶部的“大叶子”是一部光电转化器,可以把 能转化为电能。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】菱铁矿(主要成分是FeCO3)是炼铁的原料。现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如下图所示。

已知:①FeCO3+H2SO4=FeSO4+CO2↑+H2O
②菱铁矿中杂质不参加反应,且难溶于水。
请计算:
(1)20.0g菱铁矿中FeCO3的质量为 g。
(2)列式计算所用稀硫酸的溶质质量分数(结果准确到0。1%)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关微粒的说法错误的是
A.原子、分子、离子都是构成物质的微粒
B.钠原子失去1个电子形成钠离子
C.过氧化氢分子由氢分子和氧分子组成
D.构成物质的微粒是在不停地运动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com