
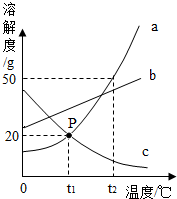
 根据如图的溶解度曲线图回答:
根据如图的溶解度曲线图回答:| 溶解度 |
| 溶解度+100g |


科目:初中化学 来源: 题型:
 把等质量的X、Y、Z、M四种金属分别加入到同体积、同浓度的足量稀盐酸中.再把M加入到YNO3溶液中.反应关系如图所示.据此判断四种金属的活动性顺序为( )
把等质量的X、Y、Z、M四种金属分别加入到同体积、同浓度的足量稀盐酸中.再把M加入到YNO3溶液中.反应关系如图所示.据此判断四种金属的活动性顺序为( )| A、Z>X>M>Y |
| B、X>Z>M>Y |
| C、X>Z>Y>M |
| D、Y>M>Z>X |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量/g | 20 | 20 | 20 |
| 生成气体质量/g | 0.08 | m | 0.04 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
 如图1所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答:
如图1所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
 某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂.该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体.
某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂.该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体.| 实验步骤 | 实验现象 |
| ①取3.00g变质粉末于一支大试管内,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体. | 固体完全溶解, |
| ②继续向上述试管中加入足量的石灰水,充分反应. | |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g. |
| 1 | Na2O2 | NaOH | Na2CO3 |
| 成分(填“有”或“没有”) | |||
| 质量(g) |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com