




 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:初中化学 来源: 题型:

| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时 的现象 |
剧烈燃烧,发出 耀眼白光,无火星 |
剧烈燃烧 极少火星 |
剧烈燃烧 少量火星 |
剧烈燃烧 火星四射 |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
 化学实验是学习化学和进行科学研究的重要方法和途径.学会气体物质的制备方法是研究气体、利用气体的基础.请根据图回答有关问题:
化学实验是学习化学和进行科学研究的重要方法和途径.学会气体物质的制备方法是研究气体、利用气体的基础.请根据图回答有关问题:| 二氧化锰 |
| 加热 |
| 二氧化锰 |
| 加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
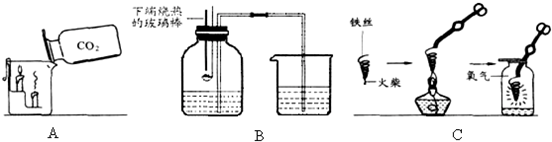
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时的现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧 极少火星 |
剧烈燃烧 少量火星 |
(未填) |
查看答案和解析>>
科目:初中化学 来源: 题型:
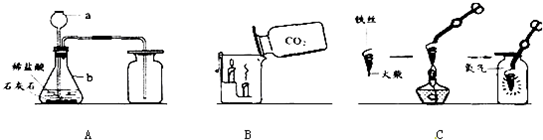
| 点燃 |
| 点燃 |
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
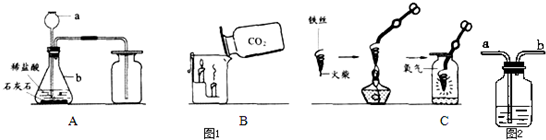
| 物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
| 燃烧时 的现象 |
剧烈燃烧,发出 耀眼白光,无火星 |
剧烈燃烧 极少火星 |
剧烈燃烧 少量火星 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com