
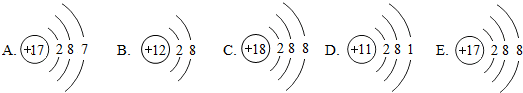
| A. | 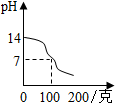 | B. | 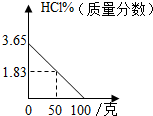 | ||
| C. | 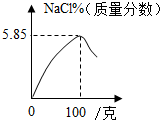 | D. | 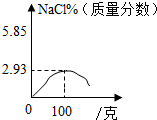 |
分析 向100克3.65%的盐酸中,逐滴加入4%氢氧化钠溶液,盐酸反应完全后,则再继续加入氢氧化钠溶液,则氢氧化钠溶液过量,则混合溶液为碱性,而氯化钠也不再生成.此题注意计算溶液的质量分数为总溶液的质量分数.
解答 解:根据氢氧化钠溶液与盐酸的反应HCl+NaOH=NaCl+H2O,则可知盐酸与氢氧化钠的反应比值:36.5:40,故可知:
A、盐酸呈酸性,pH小于7,氢氧化钠呈碱性,pH大于7,向盐酸中逐滴加入氢氧化钠溶液,pH由小于7逐渐到大于7,观察选项,故A图错误;
B、由氢氧化钠溶液与盐酸的反应HCl+NaOH=NaCl+H2O,可知,50克4%氢氧化钠溶液与盐酸反应时,混合溶液的质量为150,故HCl的质量分数一定不为1.83%,故B图错误;
C、向100克3.65%的盐酸中,逐滴加入100克4%氢氧化钠溶液时,二者完全反应,此时的氯化钠的质量分数最大,而混合溶液的质量为200克,故质量分数为5.85%错误,故C错误;
D、向100克3.65%的盐酸中,逐滴加入100克4%氢氧化钠溶液时,二者完全反应,此时的氯化钠的质量分数最大为2.93%,而继续加入氢氧化钠溶液,则其质量分数变小,故D正确.
故选D.
点评 本题考查了常见物质的性质,完成此题,可以依据已有的知识进行.分析时要注意D选项的横坐标是盐酸的质量,开始时应该用盐酸的量进行计算


科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中, 滴加稀盐酸 | 有气泡冒出 | 该溶液是碳酸钠溶液, 有关反应的化学方程式为: Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
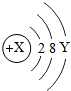 为某元素的粒子结构示意图,若为原子,则X-Y等于10.若X-Y等于8,则该粒子的符号是S2-.
为某元素的粒子结构示意图,若为原子,则X-Y等于10.若X-Y等于8,则该粒子的符号是S2-.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
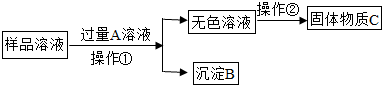
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
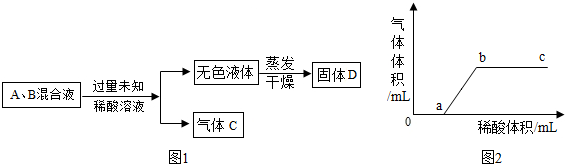
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 糖类 | B. | 蛋白质 | C. | 纤维素 | D. | 无机盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全溶解,再加入过量氯化钡溶液; | 生成白色的沉淀 | 丙的猜想不成立 |
| 2 | 取步骤1反应后的溶液与试管中滴加无色的酚酞试液 | 无明显现象 | 只有甲的猜想成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com