
下列物质中,属于纯净物的是( )
A. 空气 B. 蒸馏水 C. 生铁 D. 大理石
B 【解析】A、空气中含有氧气、氮气、二氧化碳等物质,属于混合物,错误;B、蒸馏水是由一种物质组成,属于纯净物,正确;C、生铁中含有铁和碳,属于混合物,错误;D、大理石主要成分是碳酸钙,还含有其他杂质,属于混合物,错误。故选B。科目:初中化学 来源:广东省汕头市潮阳区铜盂镇2018届九年级下学期3月阶段考试化学试卷 题型:填空题
我们生活在物质的世界里,人类的生活和生产都离不开金属。
(1)下列矿石的主要成分属于氧化物的是______(填字母)

(2)铁是应用最广泛的金属.
①生活中用铁锅做炊具,利用了铁的__________性;铁的合金有生铁和不锈钢,二者的含碳量不同:生铁________不锈钢(填“>”或“<”)
②铁制品锈蚀的过程,实际上是铁跟空气中的____________等发生了化学反应。为防止铁制栏杆生锈,通常采取的措施是________________________(写一条)。
A、C 导热 > O2和H2O 刷漆等 【解析】本题考查了铁的性质和防止铁生锈的方法。 (1)赤铁矿石的主要成分Fe2O3、铝土矿的主要成分是Al2O3,由两种元素组成,其中一种元素是氧元素,属于氧化物,故选AC; (2)①利用铁做炊具,利用了铁的导热性;铁的合金有生铁和不锈钢,二者的含碳量不同:生铁>不锈钢; ②铁制品锈蚀的过程,实际上是铁跟空气中的O2和H2O等发生了化...查看答案和解析>>
科目:初中化学 来源:江苏省2018届九年级下学期中考第一次模拟考试化学试卷 题型:填空题
生活中的化学。
(1)按要求写出下列物质的化学式:
①最常用的溶剂_______________________ ②炉具清洁剂中的碱_________________
③可用于食品干燥剂的氧化物___________ ④汽水中的一种酸___________________
(2)人们的生活离不开化学,请用化学知识回答以下问题:
①矿泉水、蔬菜、大米、禽蛋和植物油中,富含蛋白质的是:___________________;
②小明的奶奶得了夜盲症,原因是缺乏:___________________;
③多步行、骑单车出行,能有效减少CO2、CO、SO2等气体的排放,其中能引起温室效应的是:_________________;
④下列对水源的净水措施合理的顺序为:________________(填序号)。
a、加热煮沸 b、消毒 c、过滤 d、自然沉降
H2O NaOH CaO H2CO3 禽蛋 维生素A CO2 dcba 【解析】(1)①最常用的溶剂水,化学式为H2O;②炉具清洁剂中的碱是氢氧化钠,化学式为NaOH;③可用于食品干燥剂的氧化物是氧化钙,化学式为CaO ④汽水中的一种酸是碳酸,化学式为H2CO3; (2) ①矿泉水中含有水和无机盐、蔬菜中富含有维生素、大米中富含有糖类、禽蛋中富含有蛋白质,植物油中富含有油脂,故填禽蛋;...查看答案和解析>>
科目:初中化学 来源:吉林省德惠市2018届九年级下学期第一次月考化学试卷 题型:实验题
根据下列装置和仪器的示意图,回答下列问题。

(1)图中仪器A的名称_________;
(2)写出实验室制取二氧化碳的化学方程式_______________,要制取8.8g CO2需要_______g含碳酸钙80%的大理石;若要制取并收集较多的CO2,应选择的仪器有F、C、____(填序号);
(3)上述装置,还可用于实验室制取氧气,反应后要过滤分离出二氧化锰,除了烧杯,玻璃棒外,还需补充的玻璃仪器名称是________。
锥形瓶 CaCO3+2HCl=CaCl2+H2O+CO2 25 ; AHJ 漏斗 【解析】(1)仪器A是锥形瓶;(2)实验室制取二氧化碳的反应物是碳酸钙和盐酸,生成物是氯化钙、水、二氧化碳,方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;该反应不需加热,要制取较多的气体,则发生装置可选较大的发生容器锥形瓶,因为题目中给出了长颈漏斗,说明用双孔塞,收集气体需要集气瓶,由于二氧化碳...查看答案和解析>>
科目:初中化学 来源:吉林省德惠市2018届九年级下学期第一次月考化学试卷 题型:单选题
下列实验方案中,设计合理的是( )
A. 制取少量的氢氧化铜:将Ba(OH)2溶液和CuSO4溶液混合后过滤
B. 除去N2中混有的水蒸气和CO2:将气体依次通过浓硫酸、石灰水
C. 鉴别NaOH和NaCl:取等量样品,分别溶于适量水中,测温度变化
D. 检验氢氧化钠部分变质:取样,滴加适量的氢氧化钙溶液后,过滤,向滤液中再滴加酚酞溶液
C 【解析】A、Ba(OH)2溶液和CuSO4溶液混合后发生复分解反应生成氢氧化铜蓝色沉淀和硫酸钡白色沉淀,实验设计不合理,错误;B、除去N2中混有的水蒸气和CO2:将气体依次通过氢氧化钠、浓硫酸,实验设计不合理,错误;C、鉴别NaOH和NaCl:取等量样品,分别溶于适量水中,氢氧化钠溶于水放出热量,氯化钠溶于水温度无明显变化,故测温度变化鉴别,实验设计合理,正确;D、氢氧化钠和氢氧化钙均为...查看答案和解析>>
科目:初中化学 来源:山东省邹城市四校2018届九年级3月学情检测化学试卷 题型:计算题
某同学为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
①称取25.0g石灰石样品,平均分成两份,并分别加工成块状和粉末状;
②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如下图所示。请回答:

(1)由图中曲线分析得出,影响该化学反应速率的因素是:__________;
(2)每份样品充分反应后.生成二氧化碳的质量为____________.
(3)若每份样品中加入l00.0g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数为_____________。(要求写出计算过程.不考虑水、氯化氢的逸出.结果精确到0.1%)
反应物间的接触面积 4.4 g 10.5% 【解析】(1)反应物间的接触面积越大,反应速度越快。(2)根据图像可知,每份样品充分反应后.生成二氧化碳的质量为4.4 g 。(3)设恰好完全反应时生成氯化钙的质量为x,每份石灰石样品所含碳酸钙的质量为y。 CaCO3 + 2HCl == CaCl2 + H2O + CO2↑ 100 111 44 y x 4.4 g =,解...查看答案和解析>>
科目:初中化学 来源:山东省邹城市四校2018届九年级3月学情检测化学试卷 题型:单选题
向一定量的盐酸和氯化钙混合溶液中逐滴滴入碳酸钠溶液,且参加反应的碳酸钠溶液的质量与生成沉淀的质量之间的关系如图所示。则下列说法正确的是 ( )
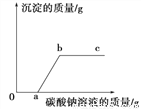
A. 反应过程中没有气泡
B. a点所处状态的溶液中溶质只有一种
C. b点比c点所处状态的溶液中氯化钠的质量分数小
D. ab线段上任意一点对应溶液的pH=7
D 【解析】A. 碳酸钠能与盐酸反应产生气体而冒气泡,错误;B. a点是碳酸钠恰好把盐酸反应完,溶液中的溶质有生成的氯化钠、没参与反应的氯化钙,错误;C. b点是混合溶液中的物质与碳酸钠恰好反应完,c点是碳酸钠过量,两点溶液中氯化钠的质量相等,但c点溶液质量比b点溶液质量大,故c点溶液的溶质质量分数小,错误;D. ab线段表示碳酸钠溶液与氯化钙溶液发生反应,Na2CO3 + CaCl2 ==...查看答案和解析>>
科目:初中化学 来源:重庆市2018届九年级下学期第一次月考化学试卷 题型:填空题
锂广泛应用于电池、贮氢等领域,锂在化合物中显+1价。如图周期表中的信息及4种粒子的结构示意图。

(1)B、C、D、E 中,____(填编号)属于离子。
(2)LiMnO2 是一种电极材料,其中 Mn 的化合价为_________。
(3)用化学符号表示:① 锂离子______; ② 氢氧化锂_______。
D +3价 Li+; LiOH 【解析】(1)根据粒子结构示意图中核内质子数不等于核外电子数属于离子进行分析;(2)根据在化合物中正负化合价代数和为零,结合LiMnO2的化学式进行解答本题;(3)根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。若表示多个该离子,就在其元素符号前加上相应的数字,进行解答;据物质化学式...查看答案和解析>>
科目:初中化学 来源:江苏省高邮市2018届九年级下学期第一次月考化学试卷 题型:综合题
工业废料石膏(CaSO4•2H2O)可以“变废为宝”,用于生产氧化钙、硫酸钾、电石(化学名称为碳化钙)等。某研究性学习小组展开了如下系列研究。
一、高纯CaO的制备
【资料一】
Ⅰ.石膏(CaSO4•2H2O)与碳粉高温煅烧生成氧化钙和几种气态非金属氧化物。
Ⅱ.SO2能使品红溶液褪色,也能使澄清石灰水变浑浊。
甲同学用如图1装置制备CaO并验证石膏与焦炭高温反应的其他产物。

实验过程中发现:B中无水硫酸铜变蓝;C中产生__现象证明有SO2生成;装置__中无明显变化和装置F中__现象证明有CO2生成。写出石膏与碳粉在高温条件下反应的化学方程式:____。
二、硫酸钾和电石的制备
乙同学模拟生产化肥硫酸钾和电石的流程如图2:

【资料二】CaO与C在高温下反应生成碳化钙(化学式为CaCx)和CO。
(1)反应①的化学方程式为___。证明固体M中不含CaCO3的方法是____(写出实验的方法、现象)。
(2)反应②的化学方程式为(NH4)2SO4+2KCl═K2SO4↓+2NH4Cl,该反应能析出K2SO4晶体的原因是__。
三、假设上述流程中制得的碳化钙(化学式为CaCx)固体中只含杂质CaO,乙小组同学为测定CaCx中x的值进行如下实验。

【资料三】CaCx在空气中灼烧生成CaO和CO2。
步骤一:称取3.76g样品于图3所示石英管中(测定装置图如图3,夹持及加热装置省略),反应前缓缓通入空气,高温灼烧石英管中的样品至反应完全后继续缓缓通入空气,测得丙溶液的质量比反应前增重了4.4g。(玻璃纤维可防止固体粉末进入导管)
步骤二:将石英管内剩余固体全部转移到水中,加入足量碳酸钠溶液,经搅拌、过滤、洗涤、干燥等操作得到碳酸钙固体6克。试回答下列问题:
(1)装置甲的作用是__。反应完全后继续缓缓通入空气的目的是__。
(2)根据步骤一、二计算该样品中钙、碳、氧的质量比为___,
计算确定CaCx的化学式(请写出计算过程)______________。
(3)若碳酸钙未能完全干燥,则会导致CaCX中的x的值____(填“偏大”、“偏小”、“无影响”)。
品红溶液褪色 E 出现浑浊 2CaSO4·2H2O + C 2CaO + CO2↑+ 2SO2↑+ 4H2O↑ CaSO4 + (NH4)2CO3 ===CaCO3↓+ (NH4)2SO4 取少量固体,加入稀盐酸,无气泡生成,则无碳酸钙 相同温度下,K2SO4的溶解度小 除去通入空气中的CO2气体 将生成的CO2完全排入丙装置中吸收 【答题空10】30:15:2 CaC2 偏小 【解析】一、...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com