
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
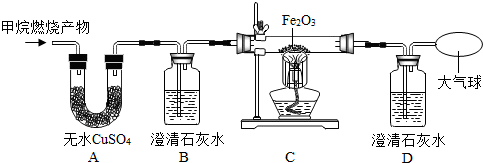
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 某溶液蒸发一定量的溶剂后有晶体析出,则原溶液一定是饱和溶液 | |
| B. | 一定温度下,向饱和溶液中增加溶剂的质量,饱和溶液一定变为不饱和溶液 | |
| C. | 某物质饱和溶液的溶质质量分数一定比它的不饱和溶液的溶质质量分数大 | |
| D. | 将30g硝酸钾放到70g水中,所得溶液的溶质质量分数不一定为30% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢气 | B. | 一氧化碳气体 | ||
| C. | 一氧化碳和氢气的混合气体 | D. | 氢气和氮气的混合气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
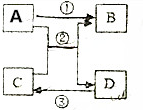 ABCD有如下转化关系,其中C为黑色粉末,D为红色固体.
ABCD有如下转化关系,其中C为黑色粉末,D为红色固体.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验 | 1 | 2 | 3 | 4 |
| 加入盐酸的质量/g | 50 | 100 | 150 | 200 |
| 剩余固体的质量/g | 8.5 | 4.5 | 2.5 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
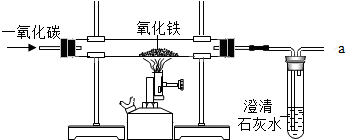 钢铁的冶炼是我国古代的化学工艺,请你参与到以下炼铁的实验中探究(一)炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见图,对实验进行分析并回答:
钢铁的冶炼是我国古代的化学工艺,请你参与到以下炼铁的实验中探究(一)炼铁的原理是利用一氧化碳与氧化铁反应,某同学利用该原理设计了一个实验,实验装置见图,对实验进行分析并回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
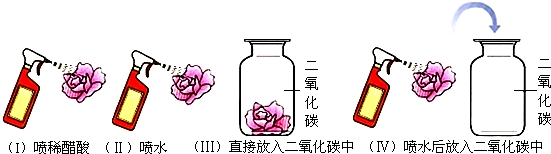
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com