
| ��Ӧǰ | ��Ӧ�� |
| ʯ��ʯ��Ʒ����6.0�� | �������������� 63.8�� |
| ϡ��������60.0�� | |
| �ձ�����100.0�� | �ձ�����100.0�� |
���� ��1�����л�ѧ��Ӧ����ѭ�����غ㶨�ɣ�
��2�����ݸ÷�Ӧ��ֻ�ж�����̼�����壬�����������غ㶨�ɺͷ�Ӧǰ���ձ������ʵ�������֮�������������̼����������������̼���������뻯ѧ��Ӧ����ʽ������̼��Ƶ��������ټ���̼��Ƶ�����������
��3�����û�ѧ��Ӧ����ʽ������Ȼ��Ƶ���������������Һ���������������ʵ���������
��� �⣺��1�����л�ѧ��Ӧ����ѭ�����غ㶨�ɣ��÷�ӦҲ�����⣻
��2���������غ��֪��������̼������Ϊ��60.0g+6.0g��-63.8g=2.2g��
��̼��Ƶ�����Ϊx�����ɵ��Ȼ��Ƶ�����Ϊy��
��CaCO3+2HCl�TCaCl2+H2O+CO2����
100 111 44
x y 2.2g
$\frac{100}{x}=\frac{111}{y}=\frac{44}{2.2g}$
���x=5g��y=5.55g��
��3�������ʼȲ�����ˮ��Ҳ�����������ʷ�Ӧ��
����Һ������Ϊ63.8g-��6.0g-5g��=62.8g��
���ʵ�����Ϊ5.55g��
�����ʵ���������Ϊ$\frac{5.55g}{62.8g}$��100%=8.8%
�𰸣�
��1����ѭ��
��2������Ʒ��̼��Ƶ�����Ϊ5g��
��3����Ӧ��������Һ���ʵ�����������8.8%��
���� ���⿼��ѧ�����û�ѧ��Ӧ����ʽ�ļ��㣬��ȷ������̼�����岢���������غ������������̼�������ǽ��Ĺؼ���


 �ο�������ϵ�д�
�ο�������ϵ�д� ������ѧ��ʱ��ҵϵ�д�
������ѧ��ʱ��ҵϵ�д� ���������ʱ��ѵϵ�д�
���������ʱ��ѵϵ�д� �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
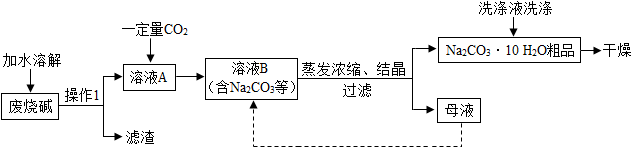
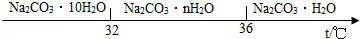
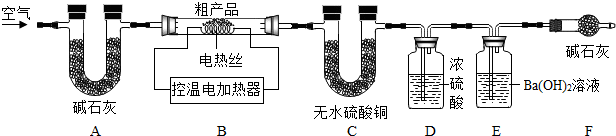
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
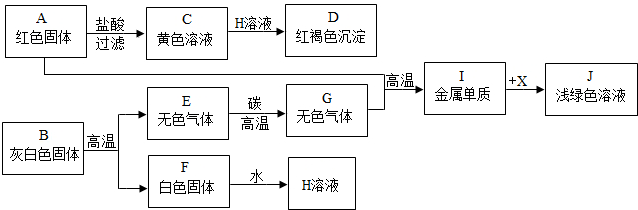
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

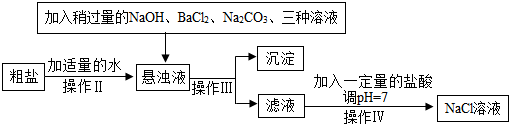
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
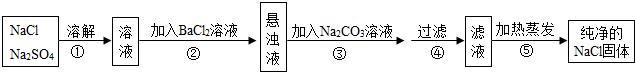
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͼ������κ�ˮ�ķ�Ӧ�����кͷ�Ӧ���������κ�ˮ�ķ�Ӧ�����кͷ�Ӧ | |
| B�� | ij��ɫ��Һ�����̪��Һ�Ժ�ɫ������Һ��һ���Ǽ����Һ | |
| C�� | ����ȼ����Ҫͬʱ��������������������Ҳ��Ҫͬʱ�ƻ����������� | |
| D�� | ��֤�ռ���Һ���Ƿ���Cl-���ȼ�ϡ�����ȥOH-���ټ�AgNO3��Һ���а�ɫ�������֣�֤������Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ���ڵ��ʣ�����ʡ����������
���ڵ��ʣ�����ʡ�����������鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com