
分析 根据质量守恒定律,生成二氧化碳的质量=反应前物质质量总和-反应后物质质量总和;然后利用碳酸钠与盐酸反应的化学方程式和生成二氧化碳的质量,列出比例式,就可计算出参加反应的纯碱(碳酸钠)的质量,再根据质量分数公式计算即可.
解答 解:根据质量守恒定律,生成CO2的质量为:12.0g+5×10g-57.6g=4.4g,
设参加反应的纯碱的质量为x,
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
x=10.6g
样品中碳酸钠的质量分数=$\frac{10.6g}{12g}×$100%≈88.3%
答案:
(1)12.0g样品与足量稀盐酸反应产生气体的质量为4.4g
(2)样品中碳酸钠的质量分数为88.3%
点评 本题有一定的难度,主要是原产品的质量,计算中用到了关系式解法和根据化学方程式进行求解,是一道不错的试题.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 1.用药匙尾端挑一点氢氧化钙粉末,分别加入A、B两支试管中,各加1mL水振荡 | 两试管中液体均呈白色浑浊状态 | 不填 |
| 2.在A试管中再加少量水振荡试管;向B试管中加入少量浓盐酸,振荡试管 | A试管中液体仍然呈白色浑浊状态.B试管中 白色浑浊消失成为无色溶液 | 氢氧化钙难溶于水;氢氧化钙能与盐酸反应生成易溶物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
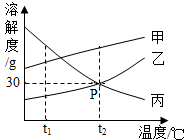 甲、乙、丙三种物质的溶解度曲线如图所示,请根据图回答下列有关问题:
甲、乙、丙三种物质的溶解度曲线如图所示,请根据图回答下列有关问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 常用于淡化海水的方法有蒸馏法、过滤法等 | |
| B. | 粗盐提纯为较纯净的食盐晶体的操作为:溶解、过滤、蒸发 | |
| C. | 通常在苦卤中加入熟石灰制取氢氧化镁 | |
| D. | 海水中的食盐用途广泛,例如侯德榜利用食盐为原料制得了纯碱 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是a、b、c三种物质的溶解度曲线.下列说法正确的是( )
如图是a、b、c三种物质的溶解度曲线.下列说法正确的是( )| A. | t1℃时,a、c的饱和溶液溶质质量分数为20% | |
| B. | t2℃时,将100 g a物质加入到100 g水中形成溶液的溶质质量分数为50% | |
| C. | t1℃时,质量相等的a、b、c三物质的饱和溶液中水的质量大小关系是a=c>b | |
| D. | t2℃时,将a、b、c三物质的饱和溶液分别降温到到 t1℃时,三种溶液中溶质质量分数的大小关系是b>a=c |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com