
分析 (1)①、过氧化氢是由氢元素和氧元素构成;
②、根据过氧化氢的组成分析;
③、根据过氧化氢的构成分析;
④、根据元素只讲种类不讲个数分析;
(2)根据过氧化氢的组成分析;
(3)①根据用质量分数为10%的H2O2溶液质量分数为5%的H2O2溶液的操作分析用到的仪器;
②根据溶质质量不变分析计算;
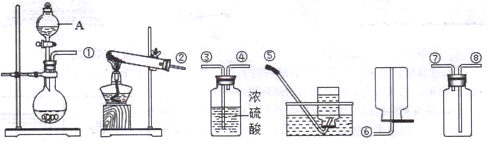
(4)要收集干燥的氧气应用向上排气法收集,不能用排水法收集,氧气中的水蒸气可用浓硫酸来干燥,据此分析连接的顺序.
解答 解:(1)①过氧化氢是一种纯净物,它是由氢元素和氧元素组成的,不含氢气和氧气,故①错误;
②过氧化氢是由氢元素和氧元素组成的,故②正确;
③每个过氧化氢分子是由2个氢原子和2个氧原子构成的,不含有氧分子和氢分子,故③错误;
④元素只讲种类不讲个数,故④错误;
(2)过氧化氢是由一种物质组成的,属于纯净物,该纯净物是由两种元素组成的,属于化合物,其中一种元素是氧元素,属于氧化物;
(3)①若用质量分数为10%的H2O2溶液(密度已知),配制680g质量分数为5%的H2O2溶液做消毒液,应量取10%的H2O2溶液和水,应用到量筒、胶头滴管,应在烧杯中用玻璃棒搅拌溶解,所以用不到的仪器是酒精灯和漏斗;
②设需要10%的过氧化氢溶液的质量为x
x×10%=680g×5% 解得:x=340g
(4)氧气中的水蒸气可用浓硫酸来干燥,要收集干燥的氧气应用向上排气法收集,不能用排水法收集,由于氧气的密度大于空气的密度,⑧应是进气口,所以自导管编号的连接顺序依次是:①③④⑧.
故答为:(1)②.(2)纯净物、化合物、氧化物;(3)①酒精灯和漏斗;②340g;(4)①③④⑧.
点评 本题考查的知识点较多,主要考查了化学式的意义、物质的分类、溶质质量分数的计算和气体的收集干燥等知识,都属于基础的知识,难度不大,加强基础知识的学习,有利于解答本题.


科目:初中化学 来源: 题型:选择题
| A. | ①④ | B. | ①② | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
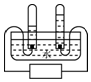 学习科学以后,我们对水有了更全面的认识.关于“水”回答下列问题:
学习科学以后,我们对水有了更全面的认识.关于“水”回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| / | Mn | Mg | Ag |
| 实验现象 | 产生气泡速率缓慢 | 产生气泡速率快 | 无任何现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 0℃ | 20℃ | 40℃ | 60℃ | |
| NaHCO3 | 6.9 | 9.6 | 12.7 | 16.4 |
| NaCl | 35.7 | 35.8 | 36.6 | 37.3 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
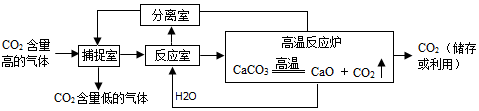
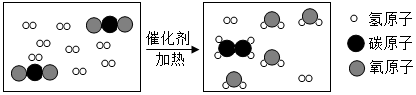
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度(℃) | 0 | 20 | 40 | 60 | 80 |
| 溶解度(克) | 12.6 | 15.3 | 20.0 | 25.0 | 25.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com