
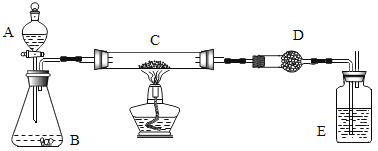
【题目】某课外活动小组加热炭粉(过量)和氧化铜的混合物,再用下图所示装置,对获得的铜粉(含炭)样品进行实验。图中铁架台等装置已略去。请你帮助他们完成下列实验报告。
(实验用品)
仪器:天平、分液漏斗、锥形瓶、硬质玻璃管、干燥管、酒精灯、洗气瓶等。
药品:红褐色(含炭)样品、过氧化氢溶液、二氧化锰、碱石灰(固体氢氧化钠和氧化钙的混合物)、浓硫酸等。
(实验内容)
实验步骤 | 实验现象 | 有关化学方程式 |
在C中加入样品粉末W g,D中装入药品后并称量为m1 g,连接好仪器。 | ||
打开A的上塞、活塞,慢慢滴加溶液。 | ________ | ________ |
对C进行加热。当C中药品充分反应后,关闭A的活塞,停止加热。 | ________ | ________ |
冷却后,称量D的质量为m2 g。 |
(计算)
样品中铜的质量分数=_______________________(用含W、m1、m2的代数式表示)。
问题和讨论:实验完成后,老师评议说:按上述实验设计,即使C中反应完全,D中吸收完全,也不会得出正确的结果。经讨论,有同学提出在B与C之间加入一个装置。再次实验后,得到了较正确的结果。那么,原来实验所测得的铜的质量分数偏小的原因可能是_________________________。
【答案】B、E中有气泡产生 2H2O2![]() 2H2O+O2↑ C中的红褐色粉末变成黑色 2Cu+O2
2H2O+O2↑ C中的红褐色粉末变成黑色 2Cu+O2![]() 2CuO ,C+O2
2CuO ,C+O2![]() CO2
CO2 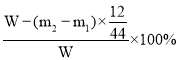 水蒸气通过C后被D中碱石灰吸收
水蒸气通过C后被D中碱石灰吸收
【解析】
实验内容:
B中装的是二氧化锰、A中是双氧水,所以打开A的上塞、活塞,慢慢滴加溶液,B装置是制取氧气的装置发生双氧水在二氧化锰催化作用下迅速产生氧气,C中加热发生以下两个反应:铜和氧气生成氧化铜,碳和氧气生成二氧化碳。因此:
实验步骤 | 实验现象 | 有关化学方程式 |
在C中加入样品粉末W g,D中装入药品后并称量为m1 g,连接好仪器。 | ||
打开A的上塞、活塞,慢慢滴加溶液。 | B、E中有气泡产生 | 2H2O2 |
对C进行加热。当C中药品充分反应后,关闭A的活塞,停止加热。 | C中的红褐色粉末变成黑色 | 2Cu+O2 |
冷却后,称量D的质量为m2 g。 |
计算:
C中生成的二氧化碳被D吸收,所以D实验前后增加的质量即是铜粉中的碳和氧气反应生成的二氧化碳。
设样品中碳的质量为x。
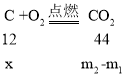
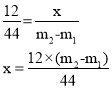
样品中铜的质量分数= 。
。
问题和讨论:
B中制得的氧气中往往含有水蒸气,水蒸气被D吸收,这样测得的D增重的质量就不仅仅是碳和氧气生成二氧化碳还有水蒸气误认为都是二氧化碳测出的碳的质量会比实际大,测出的铜的质量就会小。原来实验所测得的铜的质量分数偏小的原因可能是水蒸气通过C后被D中碱石灰吸收。


科目:初中化学 来源: 题型:
【题目】M是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组用物质M进行了如图2所示的实验.

(1)t1℃时,氯化铵的溶解度为_____g;
(2)烧杯①中溶质质量分数的计算式为_____;
(3)物质M是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组做镁条在空气中燃烧实验时,发现生成物中有黑色固体。针对这一现象,他们猜想可能是镁与N2或CO2反应生成黑色固体。
针对猜想他们开展了如下探究活动。
【实验一】镁带与氮气的反应
(1)以下是获取氮气的方法及装置,其中得到氮气较纯的是______(填字母)
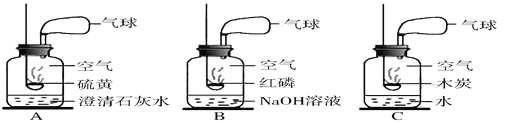
(2)燃烧镁带,观察现象
将镁带打磨光亮,点燃,伸入盛N2的集气瓶中,瓶内壁附着一层淡黄色的固体。
(3)实验结论:镁与氮气在点燃的条件下发生化合反应,生成淡黄色的氮化镁。该反应的化学方程式是:______________________________________________。
(4)实验反思:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁?原因是_____________________________________ 。
【实验二】镁带与二氧化碳的反应
将燃着的镁带伸入盛CO2的集气瓶中,镁带剧烈燃烧,瓶内产生氧化镁和一种黑色固体单质,该黑色物质是___________。(写出化学式,下同)
【探究结论】
镁在空气中燃烧产生的黑色固体是镁与空气中___________反应产生的。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高速铁路作为一种安全可靠、运载量大、低碳环保的运输方式,已经成为世界铁路发展的重要趋势,根据图示回答下列问题:
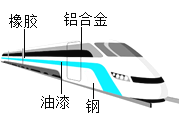
(1)图中标示的高速列车材料中,属于金属材料的是________(任写一种);
(2)高速列车使用的金属材料大多是合金而不是纯金属,这是因为合金具有更多优良性能。例如,铝合金比纯铝的硬度_______(填“大”或“小”),不锈钢锅比纯铁的抗腐蚀性_______(填“强”或“弱”)。
(3)高速列车表面喷漆除美观外,主要是为了_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在托盘天平两边各放一只烧杯并注入相同的足量稀盐酸,调节至平衡,然后向左、右两边烧杯中分别投入等质量的镁和铝,则天平指针的偏转情况是( )
A. 先偏向右,最后偏向左B. 先偏向右,最后平衡
C. 先偏向左,最后偏向右D. 先偏向左,最后平衡
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】思维导图是激发大脑潜能,练就科学思维的有效方法。图示中A~E是初中化学常见的物质,属于不同类别,C是石灰石的主要成分。图中“﹣”表示两种物质之间可以相互反应,“→”表示一种物质可以生成另一种物质。分析推理,回答问题:
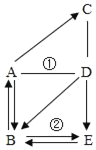
(1)物质C的化学式:_____;D→E反应的实质为_____。
(2)反应①的化学方程式:_____。
(3)反应②的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如表是NaCl和NH4Cl在不同温度时的溶解度.下列说法正确的是( )
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | 39.0 | 39.8 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 | 71.3 | 77.3 |
A.NH4Cl的溶解度受温度影响比NaCl小
B.两种物质溶解度相等的范围在10~20℃之间
C.20℃时,NaCl饱和溶液的溶质质量分数为36%
D.若NH4Cl溶液中含有少量NaCl,可采用蒸发结晶的方法提纯NH4Cl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组的同学为了研究(Cu﹣Zn合金)样品中铜的含量,取该样品20g跟足量的稀硫酸充分反应,产生氢气的质量与所用稀硫酸的质量关系如下图所示.请计算:
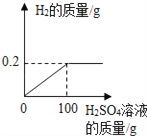
(1)反应的硫酸质量为多少g。
(2)求样品中铜的含量。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸、碱、盐在我们的生活中有着重要的作用。
(1)硫酸是一种常见的酸,下列物质不能与稀硫酸发生复分解反应的是_____(填字母)。
A NaOH溶液 B NaCl溶液 C K2CO3溶液 D Ba(NO3)2溶液
(2)氢氧化钠是一种常见的碱,聪聪同学为了探究实验室中久置的氢氧化钠固体的成分,进行了如图所示的实验。
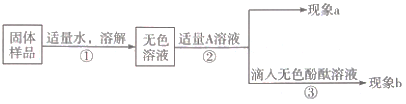
①若现象a为有气泡产生,则说明氢氧化钠已经变质,请写出产生气泡的化学方程式:_____。
②若A是Ca(OH)2溶液,现象a为有白色沉淀产生,现象b为酚酞溶液变红,该实验_____(填“能”或“不能”)说明氢氧化钠为部分变质,原因是什么_____?
(3)氯化钠是一种常见的盐,以海水为原料得到精盐NaCl和提取镁的工艺流程如图(此题中微溶物视为可溶物,所加试剂均过量)。
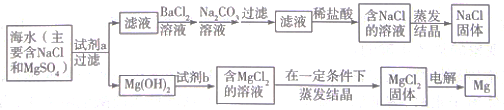
①Mg(OH)2与试剂b反应的化学方程式为_____。
②试剂a不可能是下列物质中的_____(填字母)。
A KOH溶液 B NaOH溶液 C Ca(OH)2溶液 D Ba(OH)2溶液
③在蒸发结晶的过程中,玻璃棒的作用是_____。
(4)纯碱和小苏打都是生活中常见的盐,二者性质上有一区别是小苏打受热易分解产生纯碱、二氧化碳和水,而纯碱不易分解。将25g小苏打和纯碱的固体混合物装入试管中,加热至反应完全后,可以得到18.8g固体物质。请计算原固体混合物中小苏打的质量_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com