
 某化学兴趣小组同学对某铜锌合金样品进行探究实验,称取样品10.0克放入烧杯中,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示.
某化学兴趣小组同学对某铜锌合金样品进行探究实验,称取样品10.0克放入烧杯中,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示.分析 (1)根据题意,锌与稀硫酸反应生成硫酸锌和氢气;由反应的实验情况图,完全反应后剩余固体的质量为3.5g,即铜锌合金样品中含铜的质量为3.5g;则锌的质量为10g-3.5g=6.5g;
(2)由参加反应的锌的质量,计算出生成的硫酸锌的质量和氢气的质量,进而可计算出反应后溶质的质量分数.
解答 解:(1)由反应的实验情况图,完全反应后剩余固体的质量为3.5g,即铜锌合金样品中含铜的质量为3.5g,则锌的质量为10g-3.5g=6.5g.
铜锌合金中,Zn的质量分数是$\frac{6.5g}{10g}$×100%=65%.
答:铜锌合金中,Zn的质量分数是65%;
(2)设反应生成硫酸锌的质量为X,氢气的质量为y.
Zn+H2SO4═ZnSO4+H2↑
65 161 2
6.5g x y
$\frac{65}{6.5g}=\frac{161}{x}=\frac{2}{y}$
x=16.1g,y=0.2g
反应后溶液中溶质的质量分数是=$\frac{16.1g}{6.5g+100g-0.2g}$×100%≈15.1%
答案:
(1)铜锌合金中,Zn的质量分数是65%;
(2)反应后溶液中溶质的质量分数是15.1%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析图表信息,确定铜的质量为3.5g的质量是正确解答本题的前提和关键.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:初中化学 来源: 题型:实验探究题
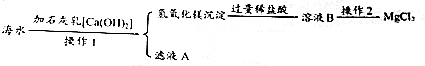
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
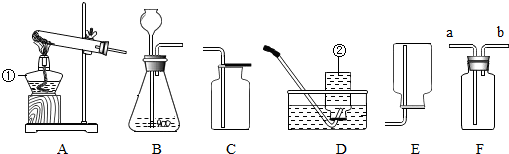
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验操作 | 实验现象 | 实验结论 |
| 用洁净试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡. | 酚酞试液变红色 | 溶液呈碱性 |
| 实验操作 | 实验现象 | 实验结论 |
| 取样品,滴入碳酸钠溶液 | 有气泡产生 | 溶液呈酸性 |
| 取样品,加入锌粒 | 有气泡产生 | |
| 取样品,滴入紫色石蕊 | 溶液变红色 | |
| 取样品,加入氧化铜 | 固体溶解,溶液变蓝色 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
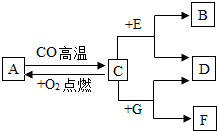 现有A、B、C、D、E、F、G七种物质,B是气体单质,C、F是常见的金属,其中F为红色,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图所示关系:
现有A、B、C、D、E、F、G七种物质,B是气体单质,C、F是常见的金属,其中F为红色,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图所示关系:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
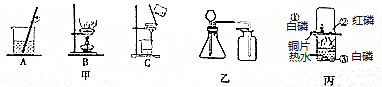
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
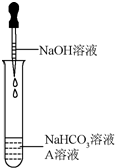 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
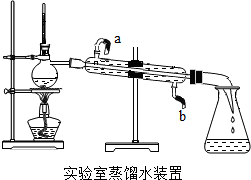 水是一种重要的自然资源.
水是一种重要的自然资源.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com