
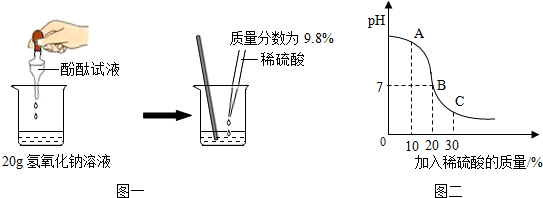
���� ��1��������ͼ�ʹ��̪��Һ�ı�ɫ����Ϳ��ǣ�
��2��A�������������ƾ���ǿ�ҵĸ�ʴ�Խ��з�����
B�������ܽ�ʱҪ�ò��������Ͻ��������
C�����ݼ���Һճ��Ƥ���ϣ����ý϶�ˮ��ϴ����Ϳ��������Һ���н��
D���������е��������Ƶ����ʽ��з�������������ƾ�����ˮ�Ժ��������̼��Ӧ�����ʣ�
��3������A����Һp����7�������
��� �⣺��1�����������Լ��ԣ���ʹ��̪��Һ��Ϊ��ɫ���������������Ʒ�Ӧ���������ƺ�ˮ�������������ԣ�����ʹ��̪��Һ��죬������Һ�ɺ�ɫ��Ϊ��ɫ��
��2��A���������ƾ���ǿ�ҵĸ�ʴ�ԣ����ܷ���ֽƬ�ϳ�����Ӧ�����ձ��Ȳ��������г������ʴ���
B���ܽ�ʱҪ�ò��������Ͻ��裬�����ܽ⣻��ȷ��
C��������������Һ����Ƥ����ʱ��Ӧ�������ô�����ˮ��ϴ��Ȼ����Ϳ��3%��5%������Һ����ϡ������и�ʴ�ԣ��ʴ���
D���������ƾ�����ˮ�ԣ���������еĶ�����̼��Ӧ�����ʣ�����Ҫ�ܷⱣ�棬����ȷ��
��3����ͼʾ��֪����a��ʱ��Һ��pH����7��˵��NaOH������������ȫ��Ӧ��û��ʣ�࣬������Һ�к��е������У�Na2SO4��NaOH��
�ʴ�Ϊ����1����Һ�ɺ�ɫ��Ϊ��ɫ����2��BD����3��NaOH��Na2SO4��
���� ���⿼��������кͷ�Ӧʱ��ҺPH�ı仯�Լ���Ӧʱ����֮���������ϵ����ɴ��⣬�����������е�֪ʶ�Լ�ͼʾ���У�����Ҫ��ͬѧ����ƽʱ��ѧϰ�м�ǿ�α�����֪ʶ�Ĵ������Ա��ܹ����Ӧ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | �� | C�� | �ط� | D�� | ���Ϸ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
| ��һ�� | �ڶ��� | ������ | ���Ĵ� | |
| ����ϡ����������g�� | 10 | 10 | 10 | 10 |
| ʣ������������g�� | 9.10 | 8.45 | 7.80 | 7.80 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ȼ�գ�4Fe+3O2$\frac{\underline{\;��ȼ\;}}{\;}$ 2Fe2O3 | |
| B�� | ������������ȼ�գ�CH4+2O2$\frac{\underline{\;��ȼ\;}}{\;}$2H2O+CO2 | |
| C�� | ����ϡ���ᷴӦ��2Fe+6HCl�T2 Fe Cl 3+3H2�� | |
| D�� | ̿��ԭ����ͭ�ķ�Ӧ��C+2 CuO�TCO2��+2Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com