

分析 (1)氢氧化钙能够吸收空气中的二氧化碳,并且能够反应生成碳酸钙和水;
(2)氢氧化钙的水溶液显碱性,能够使酚酞试液变红色;
(3)过滤可以把不溶于水的物质与谁水分开;碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
解答 解:(1)Ca(OH)2固体变质的原因是:二氧化碳与氢氧化钙在常温下反应生成碳酸钙和水,反应的化学方程式为为:CO2+Ca(OH)2═CaCO3↓+H2O.
(2)氢氧化钙的水溶液显碱性,能够使酚酞试液变红色,滴入无色酚酞溶液,观察到溶液由无色变为红色,说明假设2或假设3成立
(3)①过滤可以把反应生成的碳酸钙和水溶液分离.
②说明假设2或假设3成立,也就是证明有没有碳酸钙的存在,证明碳酸根可以加入盐酸,观察气泡.
③加入盐酸后,固体溶解,无气体生成,说明假设2成立;加入盐酸后,固体溶解,有气体生成,说明假设3成立,化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:(1)CO2+Ca(OH)2═CaCO3↓+H2O
(2)溶液由无色变为红色
(3)①过滤;②HCl; ③固体溶解,无气体生成;CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评 本题在学习氢氧化钙变质探究的基础上综合考查了氢氧化钙、碳酸钙的性质,注意把握所加入的试剂不能产生对后面的检验操作形成影响的物质,正确选择试剂,能够考查学生的知识迁移能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
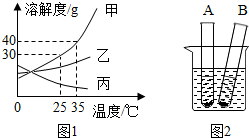 甲、乙、丙三种固体物质的溶解度曲线如图1所示,请回答:
甲、乙、丙三种固体物质的溶解度曲线如图1所示,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
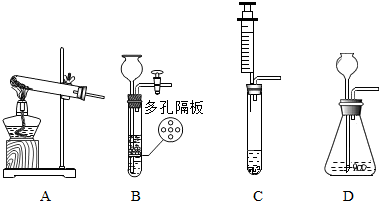
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化物:SO2C2H6O H2O | B. | 化石燃料:石油、煤、火柴 | ||
| C. | 非金属单质:磷、金刚石、汞 | D. | 混合物:矿泉水、空气、汽油 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
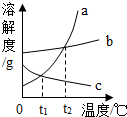 硝酸钾是初中化学重要的一种盐.请按要求填写下列有关空格:
硝酸钾是初中化学重要的一种盐.请按要求填写下列有关空格:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
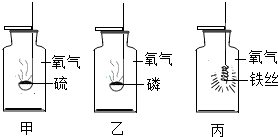 在点燃条件下进行的甲、乙、丙三个实验如图所示,根据发生反应的现象及原理,进行总结归纳并回答下列问题:
在点燃条件下进行的甲、乙、丙三个实验如图所示,根据发生反应的现象及原理,进行总结归纳并回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
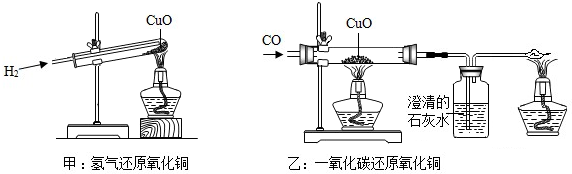
| A. | 甲实验试管口向下倾斜可防止反应生成的水倒流 | |
| B. | 乙实验只能通过澄清石灰水是否变浑浊判断反应是否发生 | |
| C. | 甲、乙两实验中,都应先使试管、玻璃管均匀受热,再通入气体,以防止发生爆炸 | |
| D. | 甲、乙两实验中,氢气和一氧化碳都将氧化铜变成游离态的铜,都发生了置换反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com