(1)用化学用语填写下列空格:
①2个氨气分子
②相对分子质量最小的氧化物
③有毒的氧化物
④能支持动物呼吸的一种单质
;
(2)有A、B、C三种元素的粒子,其核电荷数之和是36,A粒子只有一个质子(无中子电子);B粒子原子核外有18个电子,显负电性,A与B能形成化合物AB;C粒子显电中性,根据上述事实写出三种粒子的化学符号:
A
、B
、C
(3)氮化硅陶瓷是一种新型陶瓷材料,能承受高温,可用于制造业、航天工业等领域.
①氮元素与硅元素最本质的区别是
;
②由结构示意图
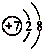
可知,氮原子最外层电子数目为
;
③工业上生产氮化硅陶瓷的方法之一是利用硅与氮气在一定条件下发生反应而制得,原料硅主要是由石英砂(主要成分是二氧化硅)与碳在一定条件下反应制得,生成物除硅外,还有一种有毒的氧化物.试写出该反应的化学方程式
.
④氮气在一般情况下不燃也不助燃,但研究发现镁在空气中燃烧产物中有少许微黄色的固体,经过研究人员测定这种微黄色的固体是镁和空气的氮气反应生成的氮化镁,现有72克的镁在氮气中充分燃烧会生成
克的氮化镁.
(4)二氧化碳若合理利用,是一种与水一样重要的原料.
Ⅰ、最近,美国研究人员利用镍和钯作催化剂,将二氧化碳转化为具有多种用途的一氧化碳或甲醇.
①该转化属于
(填“物理”或“化学”)变化;其催化剂是两种
(填“金属”或“非金属”).
②甲醇(CH
3OH)可用作赛车燃料.若其燃烧产物与蜡烛燃烧产物相同,则其化学方程式为
.
Ⅱ、日本核灾难后,清洁煤电受到追捧.我国已成功运行燃煤电厂二氧化碳捕集技术,使液态二氧化碳成为最终产品.以二氧化碳为原料可生产更环保的碳基钾肥,如碳酸钾等.碳酸钾中的阴离子是
(用离子符号表示).

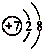 可知,氮原子最外层电子数目为
可知,氮原子最外层电子数目为