
| 反应时间 | t1 | t2 | t3 |
| 烧杯和药品质量/g | 151.3 | 151.0 | 151.0 |
分析 【结论】(1)根据质量守恒定律分析生成的氢气的质量;
(2)根据碳的质量分数计算分析判断;
【拓展】根据反应中钢的质量和碳的质量,可计算出铁的质量;结合赤铁矿中主要成分的含量,可计算赤铁矿石的质量.
解答 解:【结论】(1)由质量守恒定律可知,生成氢气的质量为:11.4g+20.0g+120g-151.0g=0.4g
(2)设钢样品中含铁的质量为x.
Fe+2HCl═FeCl2+H2↑
56 2
x 0.4g
$\frac{56}{2}=\frac{x}{0.4g}$ 解得:x=11.2g
碳的质量分数数是:$\frac{11.4-11.2g}{11.4g}×100%$=0.175%,含碳量在0.03%~0.3%之间,为低碳钢.
(3)设需要含Fe2O3 76%的赤铁矿石的质量是y
Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
y×76% 100kg(1-2%)
$\frac{160}{112}=\frac{y×76%}{100kg(1-2%)}$ 解得:y≈184.2kg.
故答为:【结论】(1)0.4.(2)是低碳钢;【拓展】(3)需要含Fe2O3 76%的赤铁矿石的质量是174.2kg.
点评 本题主要考查学生利用化学方程式进行计算的能力.解题的关键是根据质量守恒定律求出生成气体的质量,为解答打开突破口,余下的问题就可迎刃而解.


科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
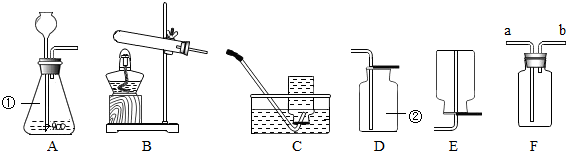
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| A. | 10℃时,将40g NaCl固体加入l00g水中,可得到l40gNaCl溶液 | |
| B. | 40℃KNO3溶液溶质质量分数一定比NaCl溶液溶质质量分数大 | |
| C. | 将30℃的KNO3饱和溶液升温至60℃,会变成不饱和溶液 | |
| D. | 20℃时,NaCl饱和溶液的溶质质量分数为36% |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
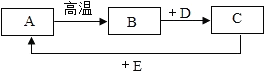 A、B、C、D、E都是初中化学常见的物质.B、D、E均为氧化物,常温下B为固态,是一种常见的干燥剂,D为液态,E为气态;A、B、C中均含有同一种金属元素.它们之间的转化关系如图所示(部分生成物略去).
A、B、C、D、E都是初中化学常见的物质.B、D、E均为氧化物,常温下B为固态,是一种常见的干燥剂,D为液态,E为气态;A、B、C中均含有同一种金属元素.它们之间的转化关系如图所示(部分生成物略去).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
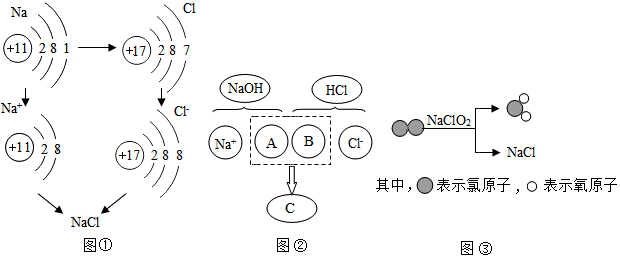
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
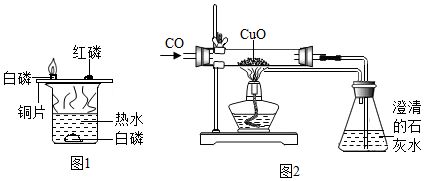
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com