
分析 依据计算公式 n=$\frac{N}{{N}_{A}}$;计算微粒数;
解答 解:3.5×6.02×1023个二氧化碳分子的物质的量=n=$\frac{N}{{N}_{A}}$=$\frac{3.5×6.02×1{0}^{23}}{6.02×1{0}^{23}}$=3.5mol;24.08×1023个氢原子的物质的量=n=$\frac{N}{{N}_{A}}$=$\frac{24.08×1{0}^{23}}{6.02×1{0}^{23}}$=4mol.
故答案为:3.5;4.
点评 本题考查了物质的量及其单位,阿伏伽德罗常数的应用,物质的量和质量、微粒数等量的换算关系,较简单,掌握基础顺利解决.


科目:初中化学 来源: 题型:选择题

| A. | ①② | B. | ①⑤ | C. | ③④ | D. | ①②⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
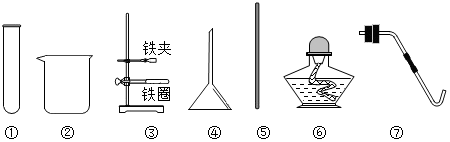
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com