

| 编号 | 实验目的 | 铁粉/g | 碳粉/g | 醋酸浓度/% |
| ① | 为以下实验作参照 | 2.0 | 0.5 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 20.0 | |
| ③ | 2.0 | 0.2 | 90.0 |
分析 (1)熟悉常见的合金的组成和用途;
(2)设计实验时要注意学会控制实验变量,从给出的数据中分析要研究的要素;
(3)最终的压强变小是要紧扣实验铁锈蚀有关,铁生锈需要消耗装置内的氧气,导致压强变小;
(4)压强改变两种情况,一是气体增大,二是温度升高,结合给定的反应进行分析.
解答 解:(1)生铁是含碳量为2%~4.3%的铁合金;
(2)实验①②是研究醋酸浓度对铁生锈速度的应影响的,所以处理醋酸的浓度不同以外,铁粉和木炭粉的质量要一样,颗粒大小也要一样,所以铁粉的质量对应也是2.0g.而①③中醋酸浓度相同,铁粉质量相同,只有杂质的量不同,所以是研究杂质对反应的影响,故填:杂质的影响.
(3)最后的压强与实验本身的目的是有关的,因为研究的是金属的锈蚀,所以要考虑到在长时间的实验中氧气和铁以及水发生的缓慢氧化消耗装置内的氧气导致压强小于起始压强;
(4)曲线图的初始阶段明显的压强增大,应该考虑气体的增多和温度的影响,气体的增多,是由于醋酸和铁反应生成了氢气,氢气的增加导致装置内的压强会明显增大.同时由于金属和酸反应是放热反应,温度的升高导致分子间间隔变大,压强也会明显增大.
故答案为:(1)2%~4.3%.
(2)2.0;杂质的影响;
(3)随着时间的进行,铁粉生锈消耗了装置内的氧气,导致压强降低.
(4)①氢气;②铁与醋酸反应放热.
点评 实验设计中既要学会从实验的实际需要出发控制变量,也要学会根据给出的数据分析要研究的实验影响因素.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
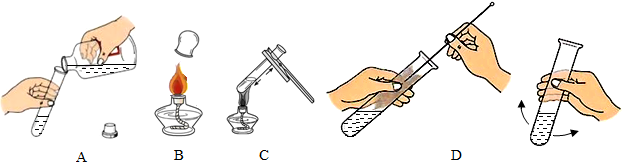
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 为了测定某品牌小苏打样品中碳酸氢钠的质量分数,兴趣小组进行了如图所示的实验(假设该样品中只含有氯化钠一种杂质),注:实验过程中发生反应的化学方程式是NaHCO3+HCl═NaCl+H2O+CO2↑.
为了测定某品牌小苏打样品中碳酸氢钠的质量分数,兴趣小组进行了如图所示的实验(假设该样品中只含有氯化钠一种杂质),注:实验过程中发生反应的化学方程式是NaHCO3+HCl═NaCl+H2O+CO2↑.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
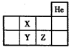 在“宏观-微观-符号”之间建立联系,是学习化学的一种重要思维方式.
在“宏观-微观-符号”之间建立联系,是学习化学的一种重要思维方式.
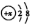 ,则x的值为8.
,则x的值为8.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
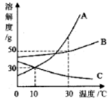
| A. | 10℃时,A、C物质的溶液中溶质的质量分数一定相等 | |
| B. | 30℃时,100g水中加入40gB物质,所得溶液为B的饱和溶液 | |
| C. | 把C的饱和溶液从30℃降温到10∁,其溶质质量分数不变 | |
| D. | 把A、B、C三种溶液从30℃降温到10℃,只有A、B析出晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com