

分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳的密度比空气大,溶于水进行分析;
(3)根据氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气进行分析;
(4)根据配制一定质量分数溶液的正确操作,以及天平的正确使用方法进行分析;
(5)根据蒸发过程的正确操作进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,②是分液漏斗;
(2)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,所以制取该气体的发生装置可选用BC,二氧化碳的密度比空气大,溶于水,所以收集二氧化碳可用D;
(3)氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)用氯化钠固体和水配制10%的氯化钠溶液,实验步骤是:计算、称量、溶解、装瓶,天平称量固体应该是左物右码,氯化钠的实际质量为:15g-3g=12g,溶剂质量为:$\frac{18g}{10%}$-18g=162g,所得溶液中氯化钠的质量分数为:$\frac{12g}{12g+162g}$×100%=6.9%;
(5)除去粗盐中不溶性杂质的实验步骤是溶解、过滤和蒸发结晶,蒸发时用到的装置是H,该装置有一处明显的错误是:没有用玻璃棒搅拌.
故答案为:(1)分液漏斗;
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑,BC,D;
(3)2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)计算,6.9%;
(5)没有用玻璃棒搅拌.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A、物质组成 | B、化学与生活 |
| ●消石灰、生石灰-化学式都是Ca(OH)2 ●蔗糖、葡萄糖、淀粉-都属于糖类物质 | ●除餐具上的油污-用洗洁精溶解 ●棉织物、羊毛织物-用灼烧闻气味来鉴别 |
| C、实验记录 | D、食品与健康 |
| ●用广泛pH试纸测定出某溶液pH值为4.2 ●用量筒量取5.25毫升水 | ●重金属中毒--喝牛奶解毒 ●人体缺碘--多吃海带、紫菜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
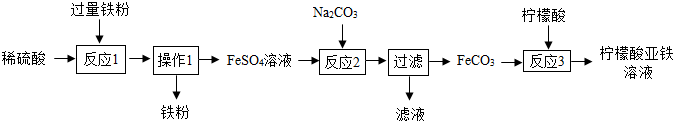
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
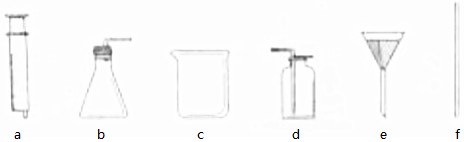
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com