

分析 (1)根据图表信息分析,一般不适合延伸,也就是从表获取信息而不能拓展;
(2)根据实验现象分析总结实验结论;
(3)铁锈的主要成分是氧化铁,能够和盐酸反应生成氯化铁和水;
(4)根据金属活动性顺序以及反应的优先原则分析;
(5)根据炼铁原理和注意事项分析,根据给出的生成的二氧化碳的质量和对应的化学方程式计算氧化铁的质量,进而求算其质量分数.
解答 解解:
(1)
A、给出的铁原子的结构示意图为四层电子,所以铁元素位于第四周期.正确;
B、原子序数也就等于核内质子数,所以铁原子核内质子数为26.正确;
C、根据给出的内容,无法确认“铁是地壳中含量最多的金属元素“.错误;
D、根据给出的信息可知,铁的相对原子质量为55.85,正确.
故选:C.
(2)将纯铜和黄铜相互刻画,由于纯铜上留下明显的划痕,说明合金硬度大于纯金属.
(3)铁锈的主要成分为氧化铁,和盐酸反应生成氯化铁和水,对应的化学方程式为 Fe2O3+6HCl═2FeCl3+3H2O.
(4)向一定量AgNO3和Cu(NO3)2的混合溶液中加入锌粉,充分反应后过滤,若滤液中只含一种溶质,则只含硝酸锌,所以应该是硝酸银和硝酸铜完全反应,则滤渣中一定含有银和铜;若滤渣只含一种金属,该金属为银,此时硝酸银是参与了反应但是不一定完全反应,所以则滤液中一定含有的金属离子是没参加反应的 Cu 2+和新生成的Zn 2+.
(5)
①由于实验用到有毒的一氧化碳,所以右边导气管口放置点燃的酒精灯的目的是 处理尾气,防止一氧化碳污染空气;硬质玻璃管中出现的实验现象是粉末由红棕色变成黑色.
②设生成二氧化碳质量为6.6g,参加反应的氧化铁的质量为x
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe
160 132
x 6.6g
$\frac{160}{132}$=$\frac{x}{6.6g}$
x=8g
赤铁矿中氧化铁的质量分数为$\frac{8g}{10g}$×100%=80%.
答:赤铁矿中氧化铁的质量分数为80%.
故答案为:
(1)C;
(2)合金硬度大于纯金属.
(3)Fe2O3+6HCl═2FeCl3+3H2O.
(4)银和铜;Cu 2+和Zn 2+.
(5)
①处理尾气,防止一氧化碳污染空气;粉末由红棕色变成黑色.
②80%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:初中化学 来源: 题型:解答题
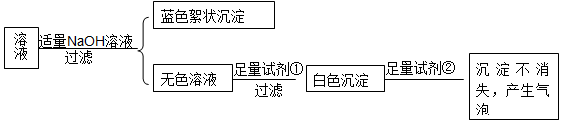
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
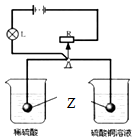 如图所示,R是滑动变阻器,它的金属滑片垂直固定在等臂金属杠杆的中央且可以随杠杆左右移动.杠杆两端分别悬挂等质量、等体积的金属锌球,此时杠杆平衡.再将铁球同时分别浸没到密度相同的稀硫酸和硫酸铜溶液中.反应一段时间后会观察到:
如图所示,R是滑动变阻器,它的金属滑片垂直固定在等臂金属杠杆的中央且可以随杠杆左右移动.杠杆两端分别悬挂等质量、等体积的金属锌球,此时杠杆平衡.再将铁球同时分别浸没到密度相同的稀硫酸和硫酸铜溶液中.反应一段时间后会观察到:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验目的 | 实验设计 | |
| A | 将铁粉和铜粉分离 | 用磁铁吸引 |
| B | 除去水中含有的杂质 | 沉淀、过滤、吸附、蒸馏 |
| C | 检验二氧化碳 | 将气体通入澄清石灰水 |
| D | 鉴别盐酸、NaCl溶液和NaOH溶液 | 分别向三种溶液中滴加几滴无色酚酞 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加速溶解 | B. | 引流 | C. | 加快蒸发 | D. | 防止液体溅出 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
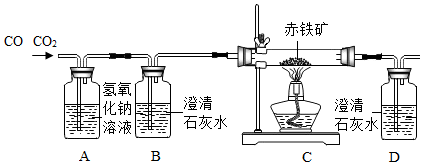
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
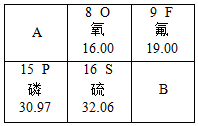 如图是元素周期表中的一部分信息,请回答:
如图是元素周期表中的一部分信息,请回答: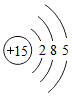 ,则磷元磷位于元素周期表的第三周期;
,则磷元磷位于元素周期表的第三周期;查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CaO (CaCO3 ) 滴加适量的稀盐酸 | |
| B. | N2( O2) 将气体通过灼热的CuO | |
| C. | FeCl2 溶液( CuCl2) 加入适量的铁粉 | |
| D. | CO2 (H2O) 将气体通过NaOH固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 剩余固体为混合物 | |
| B. | 反应后生成CO2的质量为3.1g | |
| C. | 原混合物中NaHCO3和Na2CO3质量比为21:29 | |
| D. | 反应前后的固体分别与相同浓度稀盐酸恰好完全反应所需盐酸质量相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com