


科目:初中化学 来源:不详 题型:实验题

| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 | 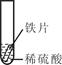 | 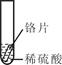 | 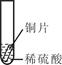 |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | ______ |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 实验编号 | 1 | 2 | 3 |
| 实验前(g) | 2.00 | 2.00 | 2.00 |
| 实验后(g) | 0.43 | 0.44 | 0.45 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 实验操作 | 实验现象 | 实验结论 |
| | 没有沉淀产生。 | 该液体不是硫酸钠溶液。 |
| | | 该液体是氯化钠溶液。 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 实验现象 | 结论 |
| 取白色沉淀甲,滴加足量的稀盐酸 | 沉淀消失 | 白色沉淀甲中一定含有 |
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取无色滤液乙,加入碳酸钠溶液 | 无明显现象 | 无色滤液乙中一定不含氯化钡 |
| 2 | 取适量无色滤液乙,加入过量的 溶液,过滤 | 生成白色沉淀 | 无色溶液中一定含有碳酸钠 |
| 3 | 取实验步骤2中的滤液,滴加 溶液 | | 原固体样品中一定存在氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 实验现象 | 实验结论 | 有关化学方程式 |
| 取少量滤液于试管中,加入足量CaCl2溶液 | | 猜想③成立 | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
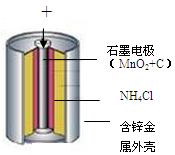

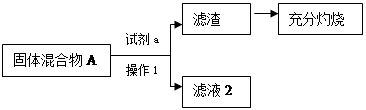
 (1)小王同学认为试剂a为水,你认为能不能实现实验目的?答: 。
(1)小王同学认为试剂a为水,你认为能不能实现实验目的?答: 。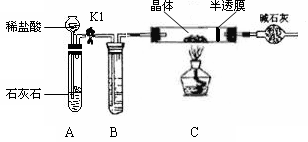
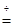 ZnSO4 + xH2O),冷却至常温后,称量玻璃管中固体其质量为16.1g。
ZnSO4 + xH2O),冷却至常温后,称量玻璃管中固体其质量为16.1g。| A.浓硫酸 | B.硝酸银溶液 | C.饱和碳酸钠溶液 | D.澄清石灰水 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
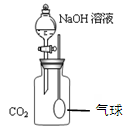
 方案二:打开瓶塞,向实验一所得的溶液中加入CaCl2溶液,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。
方案二:打开瓶塞,向实验一所得的溶液中加入CaCl2溶液,若观察到有白色沉淀产生,证明有新物质Na2CO3生成。查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com