
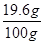 ×100%=19.6%。
×100%=19.6%。

科目:初中化学 来源:不详 题型:单选题

| A.0-t1时段,产生氢气的质量锌比铁大 |
| B.0-t1时段,产生氢气的速率锌比铁大 |
| C.0-t2时段,参加反应的锌的质量与铁相同 |
| D.0-t2时段,锌、铁消耗的盐酸质量相同 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
 Ti + 2MgCl2是金属钛冶炼过程中的反应之一。若生产4.8 t金属钛,需要金属镁的质量是多少?
Ti + 2MgCl2是金属钛冶炼过程中的反应之一。若生产4.8 t金属钛,需要金属镁的质量是多少?查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题

查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:初中化学 来源:不详 题型:计算题
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 盐酸的质量/g | 25 | 25 | 25 | 25 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com