


科目:初中化学 来源: 题型:阅读理解
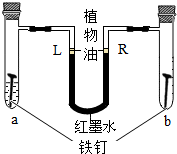 汽车作为一种常见交通工具,已走进千家万户.请回答下列问题:
汽车作为一种常见交通工具,已走进千家万户.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
| 实 验 过 程 | 实验现象 | 实 验 结 论 |
| 向盛有少量NaCl溶液的试管中滴入酚酞试液,振荡 | 溶液无明显 变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
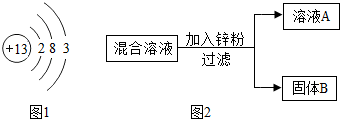 (2013?朝阳区一模)金属结构和性质等是化学研究的重要内容.
(2013?朝阳区一模)金属结构和性质等是化学研究的重要内容.
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com