
分析 (1)根据信息判断反应物、生成物、反应条件,然后写出方程式.
(2)根据质量守恒定律的实质来判断X的化学式.
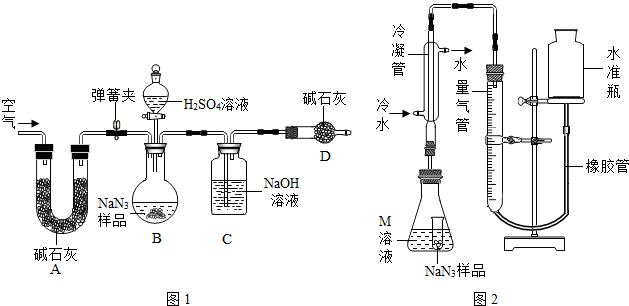
(3)根据碱石灰的成分和用途来完成第一空的解答即可,而④再打开弹簧夹,鼓入空气能将装置中残留的二氧化碳全部排入BC装置,根据氢氧化钠溶液可以和二氧化碳反应的性质来完成⑤解答.
(4)根据出现液面差后,如装置严密,装置内的气压不变的情况回答.
(5)先根据体积和密谋计算氮气的体积,再利用关系式2NaN3→3N2计算NaN3样品的纯度.
解答 解:(1)汽车经撞击后,30毫秒内引发NaN3迅速分解为Na、N2,即反应物是NaN3,生成物是Na、N2,条件是撞击,所以反应方程式为 2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑.
(2)根据质量守恒定律,反应前后原子的种类和数目不变,可确定气体X的化学式为:NH3.
(3)碱石灰的主要成分是氧化钙和氢氧化钠,二者既能吸收水分,又能吸收二氧化碳气体,所以A的作用是除去空气中的二氧化碳和水蒸气;④再打开弹簧夹,鼓入空气能将装置中残留的二氧化碳全部排入BC装置,计算碳酸钠含量,要知道样品的质量、反应前后C装置的质量,共3个数据;装置C后的球型干燥管可阻止外界的二氧化碳进入C中,如不用装置C后的球型干燥管装置,则得到的碳酸钠的含量偏大.
(4)连接好装置,从水准瓶注水,量气管中液面与右边液面形成高度差,做好标记,一段时间后,如装置严密,装置内气压不变,两边高度差不变.
(5)生成氮气的质量为70mL÷1000mL/L×1.2g/L=0.084g.
设NaN3样品的纯度X
2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑.
130 84
X•0.140g 0.084g
$\frac{130}{X•0.140g}$=$\frac{84}{0.084g}$
解得:X=92.86%
答:NaN3样品的纯度92.86%.
故答案为:(1)2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑.
(2)NH3.
(3)吸收空气中的水分和二氧化碳气体;将装置中残留的二氧化碳全部排入BC装置;3;偏大.
(4)不变.
(5)92.86%.
点评 综合实验涉及知识面广,对学生思维能力要求高,既考查知识的识记、理解、迁移、运用,又考查分析、对比、归纳等思维能力,符合素质教育培养学生能力的要求,是中考方向,对这类题目要重点训练.


科目:初中化学 来源: 题型:选择题
| A. | Na2CO3 烧碱 盐 | B. | Ca(OH)2 熟石灰 碱 | ||
| C. | C2H5OH 酒精 氧化物 | D. | NaHCO3 小苏打 酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是由氢气和氧气组成的 | |
| B. | 正极上产生的气体与负极上产生的气体的质量比是1:2 | |
| C. | 电解水的实验可以证明原子是化学变化中的最小粒子 | |
| D. | 在电解水的实验中,每2份水分解可以生成2份氧气和1份氢气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
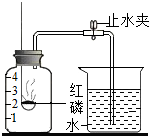 已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示.
已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
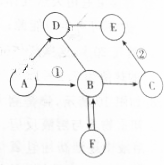 已知A、B、C、D、E、F是初中化学中常见的六种物质,其中A为一种常见的酸,B、C、D为氧化物,E为单质且粉末为黑色.F常用于建筑材料.它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“--”表示两种物质间能发生反应,部分反应物和生成物已略去).请按要求回答下列问题:
已知A、B、C、D、E、F是初中化学中常见的六种物质,其中A为一种常见的酸,B、C、D为氧化物,E为单质且粉末为黑色.F常用于建筑材料.它们之间在一定条件下有如图所示的转化关系(图中“→”表示物质间存在转化关系,“--”表示两种物质间能发生反应,部分反应物和生成物已略去).请按要求回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 蜡烛熔化,蜡烛燃烧 | B. | 水变成水蒸气,水结成冰 | ||
| C. | 铁矿石炼铁,铁器生锈 | D. | 汽油挥发,汽油燃烧 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
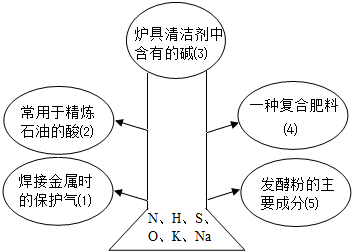 如图所示,“树”的“根部”吸收所需的“营养”元素,在“树”上开出了5朵美丽的“花朵”.请按要求填写相应“花朵”的化学式:
如图所示,“树”的“根部”吸收所需的“营养”元素,在“树”上开出了5朵美丽的“花朵”.请按要求填写相应“花朵”的化学式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com