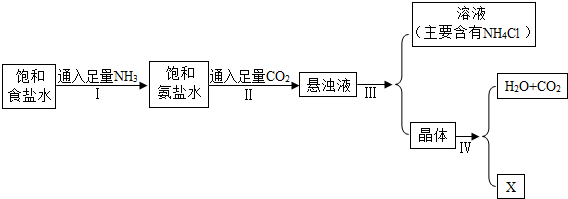
工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质.现称取只含氯化钠杂质的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g.试求:[(2)和(3)须写出计算过程]
(1)反应放出的CO2的质量为______g.
(2)该纯碱样品的纯度(计算结果精确到0.1%)
(3)所得溶液中溶质的质量分数.
【答案】
分析:(1)因为碳酸钠和盐酸反应有二氧化碳气体产生,所以反应后溶液的质量比反应前物质的总质量减少了,根据质量守恒定律可知,反应后减少的质量即为生成的二氧化碳气体的质量;
(2)根据碳酸钠和盐酸反应的化学方程式,由生成的二氧化碳的质量可得到碳酸钠的质量,进而求出纯碱样品的纯度;
(3)同样根据方程式利用二氧化碳的质量可求出生成的氯化钠的质量,最后求出反应后溶液中溶质的质量分数.
解答:解:(1)反应生成的二氧化碳气体的质量为:11g+50g+64.4g-121g=4.4g
(2)设参加反应的碳酸钠的质量为x,反应生成的氯化钠的质量为y
Na
2CO
3+2HCl═2NaCl+H
2O+CO
2↑
106 117 44
x y 4.4g
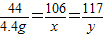
解得:x=10.6g y=11.7g
该纯碱样品的纯度为:
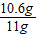
×100%=96.4%
(3)纯碱样品中所含的氯化钠的质量为:11g-10.6g=0.4g
反应后溶液中溶质氯化钠的质量为:11.7g+0.4g=12.1g
反应后溶液中溶质的质量分数为:
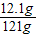
×100%=10%
故答案为:(1)4.4;
(2)该纯碱样品的纯度为96.4%.
(3)所得溶液中溶质的质量分数为10%.
点评:题是溶质的质量分数和化学方程式相结合的计算题,此题容易出错的地方是计算反应后溶液中溶质氯化钠的质量时,容易漏掉纯碱中所含的氯化钠.另外掌握住运用质量守恒计算生成气体的质量是解答此类题常用的方法.

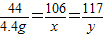
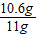 ×100%=96.4%
×100%=96.4%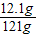 ×100%=10%
×100%=10%

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案