
分析 (1)利用金属的物理性质及用途解答此题;
(2)①分析所描述现象中的发生的反应,并写出变化中反应的化学方程式;
②根据信息写出反应的方程式;
(3)根据在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来分析.
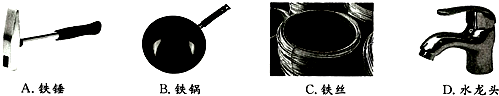
解答 解:(1)A、铁锤利用了金属的硬度;
B、铁锅利用了金属的导热性;
C、铁丝利用了金属的延展性;
D、水龙头利用了金属的硬度.
综上,故选C;
(2)①溶液变成黄色是由于铁锈与盐酸反应生成氯化铁,反应的化学方程式:6HCl+Fe2O3=2FeCl3+3H2O;有气泡放出则是由于未生锈的铁与盐酸反应产生了氢气反应的化学方程式:Fe+2HCl=FeCl2+H2↑;故答案为:6HCl+Fe2O3=2FeCl3+3H2O、Fe+2HCl=FeCl2+H2↑;
②生锈的铁制品放入过量稀盐酸中.铁锈和与稀盐酸反应生成氯化铁和水,铁与稀盐酸反应生成氯化亚铁和氢气;将上述所得溶液中,加入过氧化氢溶液反应是氯化亚铁、过氧化氢和氯化氢反应生成氯化铁和水,故反应的方程式为:2FeCl2+H2O2+2HCl=2FeCl3+2H2O;
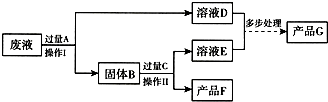
(3)①要得到铜和氧化铁这两种产品,则需要加入铁将氯化铜中的铜置换出来,故A是铁,铁能与氯化铜反应生成氯化亚铁和铜,故填:Fe+CuCl2=Cu+FeCl2;
②加入的铁过量,故将铜完全置换出来后还有铁剩余,故B是铁和铜的混合物,故填:Fe和Cu;
④要将过量的铁除去,需要加入稀盐酸,故C为稀盐酸,使铁与盐酸反应生成氯化亚铁和氢气,若要检验盐酸过量,可以取过滤得到的溶液E中加入锌粉,观察到有气泡产生,故填:取少量溶液E于试管中,加入少量锌粒,若有气泡产生,则C过量.
点评 本题考查了常见金属的性质和利用,完成此题,可以依据已有的金属的性质进行.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
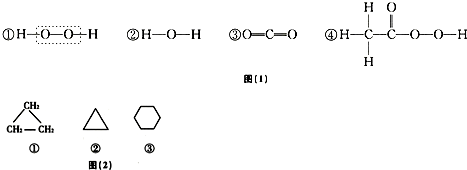
| 物质 | 水 | 铁 | 氯化钠 | 硫酸亚铁 |
| 粒子符号 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
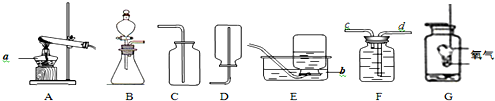
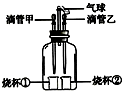 某实验装置如图所示.若先将甲中液体挤出,观察到气球明显鼓起,一段时间后,气球恢复原状,则滴管甲和烧杯①中液体物质可能是浓硫酸和水(写出1种组合,下同);再将滴管乙中的液体挤出,气球又明显鼓起,一段时间后,气球略微缩小,但不能恢复至原状,则滴管乙和烧杯②中物质可能是镁和稀盐酸.
某实验装置如图所示.若先将甲中液体挤出,观察到气球明显鼓起,一段时间后,气球恢复原状,则滴管甲和烧杯①中液体物质可能是浓硫酸和水(写出1种组合,下同);再将滴管乙中的液体挤出,气球又明显鼓起,一段时间后,气球略微缩小,但不能恢复至原状,则滴管乙和烧杯②中物质可能是镁和稀盐酸.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 红磷在氧气中剧烈燃烧,生成大量白色烟雾 | |
| B. | 硫在空气中燃烧,发出蓝紫色火焰,生成白烟 | |
| C. | 煤炭在空气中燃烧,生成二氧化碳气体 | |
| D. | 生石灰与水反应,放出热量 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 是氧化物 | B. | 由碳、氢、氧元素组成 | ||
| C. | 由分子构成 | D. | 碳、氢、氧原子个数比为7:10:5 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com