
【题目】学习《海水“制碱”》的知识后,小明在实验室中进行了如下探究活动,请你和小明一起完成下面的实验探究活动。
(1)探究碳酸钠的溶解性:在编号为 A、B、C、D 的四个烧杯中各加入室温下的水 100g,并分别加入取自实验室的碳酸钠固体,搅拌至充分溶解,实验数据记录如下表:
烧杯编号 | A | B | C | D |
水的质量/g | 100 | 100 | 100 | 100 |
加入 Na2CO3 的质量/g | 30 | 35 | 40 | 50 |
溶液的质量/g | 130 | 135 | 140 | 140 |
分析上述数据,烧杯编号为_________中的溶液是饱和溶液。
(2)探究食用纯碱的纯度:小明把家中厨房里的食用纯碱(主要成分是Na2CO3)带到实验室,他称取食用纯碱12.0g放入烧杯中,加入200g水使其完全溶解。现将150g一定浓度的CaCl2溶液逐滴滴入烧杯中,测得滴加氯化钙溶液的质量与生成沉淀的质量关系如下表:
CaCl2 溶液的质量/g | 25 | 50 | 75 | 100 | 125 | 150 |
沉淀的质量/g | 2 | 4 | m | 8 | 10 | 10 |
①m 的数值是 ______。
②计算纯碱样品中碳酸钠的质量分数______(写出计算过程,计算结果保留一位小数)。
③滴加氯化钙溶液过量的目的是______。
【答案】CD 6 88.3% 将碳酸钠完全反应
【解析】
(1)A、B、C三个烧杯中溶液的质量等于水的质量+加入的Na2CO3 的质量,说明A、B烧杯中溶液肯定为不饱和溶液,C可能为饱和溶液,又由于D中水的质量+加入的Na2CO3 的质量为150g,溶液质量为140g,等于C的质量,所以D为饱和溶液,C也为饱和溶液;
(2)①由表中信息可知,滴加氯化钙质量25g至125g之间,每增加25g,沉淀质量增加2g,所以m的值为6;
②由表中信息可知,产生沉淀的质量为10g,
设参加反应的碳酸钠的质量为x,
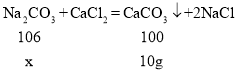
![]()
x=10.6g
纯碱样品中碳酸钠的质量分数![]()
③滴加氯化钙溶液过量的目的是将碳酸钠完全反应。


科目:初中化学 来源: 题型:
【题目】工业上可用黄铁矿(主要成分FeS2)制取硫,主要流程如下:
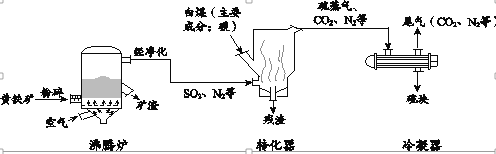
已知:沸腾炉中的主要反应为4FeS2 + 11O2 ![]() 2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
(1)黄铁矿粉碎的目的是______。
(2)在加热条件下,转化器中发生反应的化学方程式是______。
(3)冷凝器中发生的变化是______(填“物理变化”或“化学变化”)。
(4)以上流程中产生的矿渣和尾气均可再利用,其可能的用途是_____(答1条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】煤的综合利用有利于保护自然环境和社会的可持续发展。
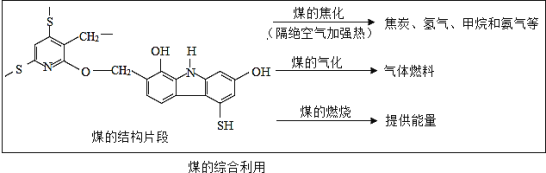
(1)由煤的结构片段可知:煤燃烧会产生大气污染,其中_____排放到空气中会导致酸雨。
(2)煤的焦化属于_____变化;焦化获得的焦炭可用于高炉炼铁,高炉内CO和Fe2O3反应的化学方程式为_____。焦化获得的氨气可用于制取氮肥,区分(NH4)2SO4和NH4Cl两种化肥可选用的试剂是_____(填对应选项的字母)。
A 熟石灰 B 氯化钡 C 盐酸
(3)焦化获得的焦炭可用于制取水煤气。我国科学家研究出碳化钼(Mo2C)负载金原子组成的高效催化体系,使水煤气中的CO和H2O在120℃下发生反应,反应微观模型如下图所示。

①从反应微观模型看,金原子对反应物_____(填化学式)起吸附催化作用。
②反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学知识可以解释许多生活生产中的问题和现象。
(1)“腌笃鲜”是苏州的一道时令美食。下列制作“腌笃鲜”的食材中,能提供蛋白质的是_________(填字母序号).
a.春笋 b.咸肉
b.咸肉 c.百叶
c.百叶 d.排骨
d.排骨
(2)很多便利店售自热小火锅,其发热的原理是利用了生石灰与水反应放热,写出发生反应的化学方程式______________,反应结束后得到的是_________液。
(3)铝制门窗比较耐腐蚀,主要原因是_______(用文字叙述)。小红还发现新买的家具带有异味,于是在室内放了几个活性炭包以达到除去异味的目的,这是利用了活性炭的______性。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】锶元素的原子结构示意图和在元素周期表中显示的信息如图所示:
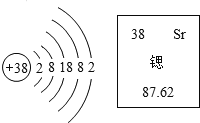
(1)锶属于______元素(填“金属”或“非金属”)。
(2)锶元素的原子序数为___________________。
(3)氧化锶的化学式是_____________,氧化锶与水能发生化合反应生成氢氧化锶并放出大量热,请你写出反应的化学方程式_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在地壳和海洋中发现的金属元素有90多种,但在日常生活和工农业生产中金属材料有几千种,可见金属材料在人类活动中占有比较重要的地位和作用。
(1)地壳中含量最高的金属元素为 _____________。
(2)炒锅利用了金属具有_________性,插座中的铜片利用金属具有____________。
(3)在加热的条件下镁能与水反应,生成氢氧化镁和某无色可燃性气体,试写出该反应的化学方程式_________________。
(4)将6.5g锌放入硝酸铜和硝酸银的混合溶液中,充分反应后过滤,所得固体的质量为6.75g,则滤液中一定含有的溶质为__________;滤渣中一定有的固体为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】《神秘岛》是儒勒·凡尔纳海洋三部曲的第三部,讲述了美国南北战争时期,被困在南军城中的几个北方人乘气球逃脱之后,飘落到“林肯岛”上求生的故事。
(1)将两片怀表上的玻璃合在一起,中部灌满水,边缘用泥粘合,制成凸透镜;用透镜集聚太阳光,照射下列物质,可以燃烧起来的是_______(填字母序号,下同)。
(2)将岛上的水生植物晒干、焚烧后,可获得Na2CO3等。Na2CO3中含有_______种元素。
(3)将赤铁矿石和木炭一层又一层叠加起来,用鼓风机吹进空气,高温加热后可以获得铁。写出一氧化碳与赤铁矿石反应的化学方程式:_______。
(4)岛上的黄铁矿(主要成分为FeS2)在空气中高温加热时生成一种有激性气味的气体,该气体可用来制造硫酸。这种气体是_______。
A.O2 B.Fe C.SO2 D. NH3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包固体,可能是Cu(NO3)2、K2SO4、KCl、K2CO3、KOH中的一种或几种组成。为了探究该固体的组成,某化学小组设计并开展以下实验:
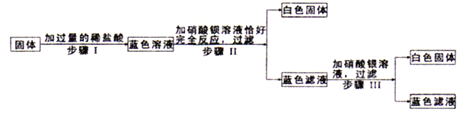
已知,步骤I中固体全部消失,溶液呈蓝色,无气泡产生,步骤II、III中均可观察到有白色沉淀生成。
请回答下列问题:
(1)经推论,原固体中一定不含K2CO3,理由是___________________
(2)原固体中一定含有的物质是________________。
(3)步骤II中产生白色沉淀的化学方程式是_______________。
(4)步骤III所得蓝色滤液中一定含有的阳离子是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化钠(Na2O2)是淡黄色的粉末,在通常状况下能跟许多物质反应。如:2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O═4NaOH+O2 2Na2O2+4HCl═4NaCl+2H2O+O2
为了验证CO2跟Na2O2反应产生的气体是O2,某同学设计了如图所示的实验装置:
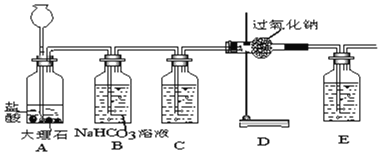
试回答下列问题:
(1)写出A中发生的化学反应的化学方程式_____。
(2)设计B、C的目的是净化CO2气体,其中B装置的作用是_____,C装置中的液体是_____,作用是_____,如果将B、C两瓶内所盛的液体互换,后果是_____ E装置的作用是_____。
(3)为了验证CO2和Na2O2反应产生的气体是O2,最后还要进行的实验操作是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com