
| a-b | ||
|
| 10(a-b) |
| 3 |
| 10(a-b) |
| 3 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
| 配料表 | 精制海盐,碘酸钾 |
| 含碘量/kg | 30mg~60mg |
| 包装日期 | 见封底 |
| 储存方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、都不能确定 |
| B、只有③能确定 |
| C、只有④⑤⑥能确定 |
| D、都能确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
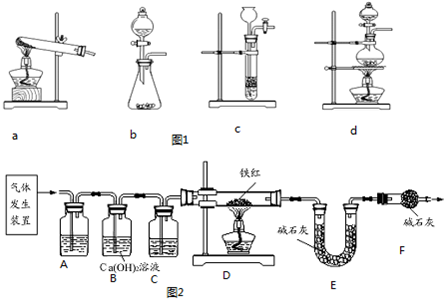
| 浓H2SO4 |
| △ |
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
查看答案和解析>>
科目:初中化学 来源: 题型:
 某校化学兴趣小组的同学们就空气中氧气的含量进行如图所示的实验探讨:
某校化学兴趣小组的同学们就空气中氧气的含量进行如图所示的实验探讨:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com