
| 溶质的化学式 | 溶质的质量/g |
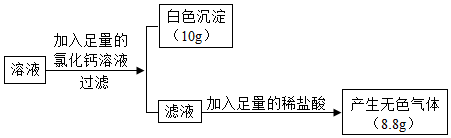
分析 根据已有的物质的性质进行分析解答,二氧化碳能与氢氧化钠反应生成碳酸钠和水,二氧化碳过量会与碳酸钠、水反应生成碳酸氢钠,据此解答;根据题干提供的数据结合化学方程式计算即可.
解答 解:【猜想假设】二氧化碳能与氢氧化钠反应生成碳酸钠和水,若氢氧化钠过量,则溶质是碳酸钠和氢氧化钠;若二氧化碳与氢氧化钠恰好反应完,则溶质是碳酸钠;若二氧化碳与氢氧化钠反应完有剩余,则溶质是碳酸氢钠和碳酸钠,若二氧化碳与生成碳酸钠恰好反应完,则溶质是碳酸氢钠,故填:Ⅲ. 有Na2CO3、NaHCO3;Ⅳ. 只有NaHCO3
.
【获得结论】反应后的溶液中加入足量氯化钙溶液,有白色沉淀生成,说明溶液中含有碳酸钠,生成的沉淀是碳酸钙,由于氯化钙足量,所以碳酸钠完全反应掉;再向滤液中加入稀盐酸,产生无色气体,说明溶液中有碳酸氢钠,由此可证明猜想Ⅲ是正确的;碳酸钠与氯化钙反应生成碳酸钙和氯化钠,反应的化学方程式为:Na2CO3+CaCl2=2NaCl+CaCO3↓.设生成碳酸钙10g需要参加反应的碳酸钠质量为Xg,则:
Na2CO3+CaCl2=2NaCl+CaCO3↓
106 100
X 10g
$\frac{106}{100}=\frac{X}{10g}$
X=10.6g
碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:HCl+NaHCO3=NaCl+H2O+CO2↑.设生成二氧化碳8.8g需要参加反应的碳酸氢钠质量为Yg,则:
HCl+NaHCO3=NaCl+H2O+CO2↑
84 44
Y 8.8g
$\frac{84}{44}=\frac{Y}{8.8g}$
Y=16.8g
故答案为:
| 溶质的化学式 | 溶质的质量/g |
| Na2CO3 | 10.6 |
| NaHCO3 | 16.8 |
点评 本题考查的是物质成分的实验探究,完成此题,可以依据已有的物质的性质结合物质间反应的实验现象进行.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
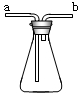 如图所示,该装置在化学实验中有洗气、检验、储气等多种用途.
如图所示,该装置在化学实验中有洗气、检验、储气等多种用途.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 化学与人类生活息息相关,学习化学的最终目的就是将其应用于生活.
化学与人类生活息息相关,学习化学的最终目的就是将其应用于生活.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20克 | B. | 30克 | C. | 40克 | D. | 无法计算 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 待区分的物质 | 鉴别方法 |
| A | 合成纤维和纯羊毛 | 分别取少量灼烧,并闻气味 |
| B | 稀硫酸和稀盐酸 | 取样,分别 AgNO3 溶液,观察是否产生沉淀 |
| C | 碳酸氢铵和氯化铵 | 闻气味 |
| D | 碳粉和氧化铜 | 取样,分别 加入足量稀硫酸,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CH2O | B. | CH4O | C. | C3H6 | D. | CH2O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com