
| A. | 14.6g | B. | 3.6g | C. | 3.2g | D. | 1.4g |
分析 根据氧化铜和稀盐酸反应生成氯化铜和水,氧化镁和稀盐酸反应生成氯化镁和水,再根据氧元素的质量守恒进行分析解答.
解答 解:由于氧化铜和氧化镁的混合物与14.6%的稀盐酸100g恰好完全反应,分析化学方程式可知氧化物中氧元素全部转变为水中的氧元素,计算出水的质量进而计算出所含氧元素的质量即可;
设氧元素的质量是x,由化学方程式可以看出稀盐酸与生成水的关系为
2HCl~H2O~O
73 18 16
100g×14.6% x
则$\frac{73}{16}=\frac{100g×14.6%}{x}$,解得x=3.2g
故选:C.
点评 本题很好的考查了质量守恒定律的应用,解答时首先分析实验的反应原理,再根据反应原理,根据化学方程式计算出该样品中某一成分的质量,得出所要探究的物质中该成分的含量.


科目:初中化学 来源: 题型:解答题
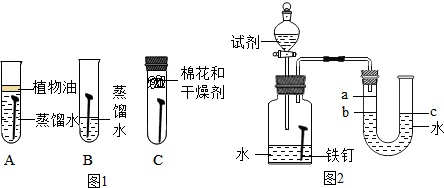
| 影响因素 | 实验设计 | 实验现象 | 实验结论及解释 |
| ①温度 | 装置Ⅰ放入25℃恒温环境中,装置Ⅱ放入40℃恒温环境中 | 两套装置中铁钉均锈蚀,且U形管中液面均由b处上升至a处,则所需时间Ⅰ>Ⅱ | 锈蚀的速率Ⅰ<Ⅱ;铁的锈蚀速率与反应时的温度有关温度越高,铁的锈蚀速度越快 |
| ②氧气含量 | 在相同温度下,装置Ⅰ集气瓶中加入氧气加入10mL乙醇 | 两套装置中铁钉均锈蚀,且U形管中液面均由b处上升至a处,则所需时间Ⅰ>Ⅱ | 铁的锈蚀速率与氧气的含量有关,氧气的含量越多,铁的锈蚀越快 |
| ③水溶液的导电性 | 在相同温度下,装置Ⅰ集气瓶中加入10mL氯化钠溶液;装置Ⅱ集气瓶中加入10mL乙醇 | 两套装置中铁钉均锈蚀;且U形管中液面均由b处上升至a处,则所需时间Ⅰ<Ⅱ | 铁的锈蚀速率与水溶液的导电性有关,在能导电的溶液中,锈蚀的速率加快 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气、水、空气、氢氧化钠 | B. | 氮气、氯酸钾、钢、醋酸钠 | ||
| C. | 可燃冰、干冰、冰水混合物、氯化锰 | D. | 石墨、生石灰、石油、小苏打 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
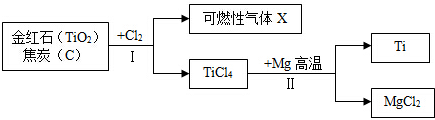
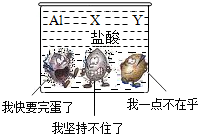
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
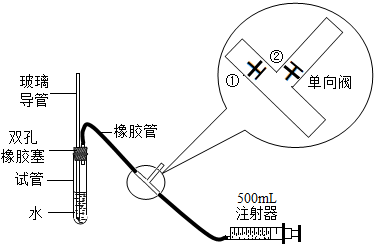
| SO2最高质量分数限值(单位:mg/m3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | X | Y | Z | W |
| 反应前质量/g | 10 | 3 | 90 | 0 |
| 反应后质量/g | 3.2 | 3 | 待测 | 3.2 |
| A. | 该反应是分解反应 | |
| B. | Y可能是催化剂 | |
| C. | 反应后Z物质的质量为86.4g | |
| D. | W和Z两种物质变化的质量比为32:36 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com