
烧杯中盛有BaCl2和HCl的混合溶液100.0g,向其中滴加溶质质量分数为10.0%的Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示。下列说法正确的是( )

A. ab段产生白色沉淀
B. bc段溶液质量增加86.3g
C. c点对应溶液的溶质质量分数为7.5%
D. 向d点溶液中滴加酚酞试液,溶液显红色
BD 【解析】 碳酸钠首先与盐酸反应生成氯化钠,水和二氧化碳,再与氯化钡反应生成氯化钠和碳酸钡白色沉淀。A、ab段产生氯化钠,水和二氧化碳,故A错误;B、bc段溶液质量增加86.3g,Na2CO3→BaCO3,106→197,﹙212g-106g﹚×10.0%=10.6g,生成碳酸钡质量是19.7g, 溶液质量增加106g-19.7g=86.3g,故B正确;C、Na2CO3→2NaCl... 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:初中化学 来源:湖北省黄石市2018届九年级5月模拟化学试卷 题型:单选题
如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )

A. 甲的溶解度大于乙的溶解度
B. 20℃时,甲、乙的饱和溶液中溶质与溶液的质量比为1:4
C. 将50℃甲物质的饱和溶液降温到30℃时,溶液质量减小
D. 将甲、乙两种物质的溶液分别从50℃降温至20℃时,溶液中溶质质量分数均为25%
C 【解析】A、没有指定温度,无法比较溶解度,错误;B、由溶解度曲线可知,20℃时,甲、乙的溶解度相等为25g,即100g溶剂中最多溶解25g溶质。因此20℃时,甲、乙的饱和溶液中溶质与溶液的质量比为25g:(25g+100g)=1:5,错误;C、由溶解度曲线可知,甲的溶解度随温度的升高而增大,故将50℃甲物质的饱和溶液降温到30℃时,有甲晶体析出,溶液质量减小,正确;D、50℃时,甲、乙两...查看答案和解析>>
科目:初中化学 来源:湖北省宣恩县2018届九年级第二次质量检测化学试卷 题型:单选题
下列变化过程中发生化学变化的是
A. 蜡炬成灰 B. 铁杵磨成针 C. 木已成舟 D. 滴水成冰
A 【解析】A、蜡炬成灰的过程中有新物质二氧化碳等生成,属于化学变化;B、铁杵磨成针的过程中只是铁的形状发生改变,没有新物质生成,属于物理变化;C、木已成舟过程中只是木材的形状发生改变,没有新物质生成,属于物理变化;D、滴水成冰过程中只是水的状态发生改变,没有新物质生成,属于物理变化。故选B。查看答案和解析>>
科目:初中化学 来源:江苏省镇江市润州区2018届九年级第二次模拟考试化学试卷 题型:填空题
钙及其化合物在生产、生活中具有广泛的应用
(一)钙及其化合物的应用
(1)青少年缺“钙”易患的疾病是________。
(2)混凝土中也含有一定量的含钙物质,钢筋与混凝土混合形成钢筋混凝土,以上叙述中不涉及的材料是_________。 a.无机材料 b.合成材料 c.复合材料
(3)即热型快餐加热原理是利用生石灰和水反应放热,用方程式表示其反应__________。
(二)过氧化钙(CaO2)的性质
(1)CaO2中氧元素的化合价为_____________。
(2)CaO2能与稀盐酸发生复分解反应,反应的化学方程式为_____________。
(3)鱼类长途运输的增氧剂的主要成分为CaO2,它与水缓慢反应生成O2,还生成一种碱,其化学式为_______,Na2O2也能与水反应,原理与CaO2相同,但却不能作为鱼虾运输的供氧剂,请分析可能的原因___________________。
(三)过氧化钙晶体的制备
(资料)过氧化钙晶体(CaO2·yH2O),常温为白色,能溶于酸,难溶于酒精。
制备原理:CaCl2+H2O2+NH3+H2O  CaO2·yH2O↓+NH4Cl,装置如下。
CaO2·yH2O↓+NH4Cl,装置如下。
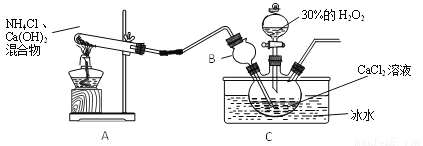
(1)装置A中试管内发生反应的化学方程式为______________________。
(2)装置C采用冰水浴控制温度在0℃左右,可能的原因主要有:
Ⅰ. 该反应是放热反应,温度低有利于提高CaO2·yH2O产率;
Ⅱ. _____________________________。
(3)反应结束后,经过滤、洗涤、低温烘干可获得CaO2·yH2O。
①洗涤时采用95%的酒精溶液洗涤的优点是_________________。
②检验晶体已洗涤干净的方法为________________________。
(四)过氧化钙晶体组成的测定
称取21.6克晶体用热分析仪对其进行热分解实验,并绘制成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水)
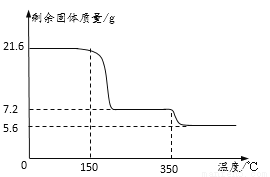
(1)0—150℃质量不发生改变的原因是______________________。
(2)根据上图可知y=________。
(3)350℃时发生反应的化学方程式为_____。
佝偻病或骨质疏松 b CaO+ H2O= Ca (OH)2 -1 CaO2+ 2HCl= H2O2+ CaCl2 Ca (OH)2 反应生成氢氧化钠,具有强腐蚀性 Ca(OH)2+2NH4Cl=CaCl2+2NH3↑+2H2O 防止过氧化氢分解 减少晶体损失,易于干燥 取最后一次洗涤所得的滤液,加入AgNO3溶液,无现象 未达到反应所需的温度 8 2CaO2 2CaO+O2↑ 【解析】(一)...查看答案和解析>>
科目:初中化学 来源:江苏省镇江市润州区2018届九年级第二次模拟考试化学试卷 题型:填空题
造雪机的工作原理如图所示。

(1)B 到 C 发生的是________变化(填“物理”或“化学”)。
(2)A 处空气被压缩,体积变小。从微粒的角度解释其原因是____________。
物理 构成空气的微粒间隔变小,空气体积变小 【解析】(1)B到C发生的是物理变化,仅是物质状态的变化,没有生成其他物质。(2)A 处空气被压缩,体积变小。从微粒的角度解释其原因是构成空气的微粒间隔变小,空气体积变小。查看答案和解析>>
科目:初中化学 来源:江苏省镇江市润州区2018届九年级第二次模拟考试化学试卷 题型:单选题
下列物质的转化在给定条件下均能实现的是
A. 
B. 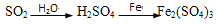
C. 
D. 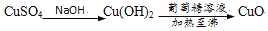
查看答案和解析>>
科目:初中化学 来源:江苏省镇江市润州区2018届九年级第二次模拟考试化学试卷 题型:单选题
用浓硫酸、水、锌粒等制取氢气并检验氢气的纯度,下列操作或装置正确的是
A.  读取液体体积 B.
读取液体体积 B. 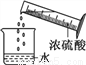 稀释浓硫酸
稀释浓硫酸
C. 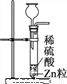 制取氢气 D.
制取氢气 D.  检验氢气纯度
检验氢气纯度
查看答案和解析>>
科目:初中化学 来源:河南省信阳市2018届九年级下学期最后一次模拟考试化学试卷 题型:单选题
实验室有碳酸钾和碳酸钙的固体混合物75g,使之与500g质量分数为14.6%的盐酸充分反应后溶液显酸性,将反应后的溶液蒸干得到83.8g固体。则原混合物中金属元素的质量分数为( )
A. 44% B. 36% C. 20% D. 55%
B 【解析】碳酸钾、碳酸钙与稀盐酸反应的化学方程式分别为CaCO3+2HCl═CaCl2+H2O+CO2↑、K2CO3+2HCl═2KCl+H2O+CO2↑,由上述化学方程式可知,碳酸钾、碳酸钙与盐酸完全反应后,可看成碳酸根离子被两个氯离子取代,两个氯离子的相对原子质量的和是71,碳酸根的相对原子质量的和是60,差是11,即完全反应后质量增加了11份质量。实际反应后固体质量增加了83.8g-...查看答案和解析>>
科目:初中化学 来源:山东省泰安市2018年中考化学试卷 题型:单选题
下列实验现象,描述错误的是
A. 电解水时正极和负极产生气体的体积比为2:1
B. 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体
C. 将一氧化碳通入灼热的氧化铁,红色粉末逐渐变为黑色粉末
D. 向硫酸铜溶液中滴加氢氧化钠溶液,产生蓝色沉淀
A 【解析】A、电解水时正极和负极产生气体的体积比为1:2,故A正确;B、 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,故B错误;C、 将一氧化碳通入灼热的氧化铁,氧化铁与一氧化碳反应生成铁和二氧化碳,红色粉末逐渐变为黑色粉末,故C错误;D、 向硫酸铜溶液中滴加氢氧化钠溶液,生成了氢氧化铜和硫酸钠,氢氧化铜是蓝色沉淀,故D错误。故选A。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com