
| A. | 全部 | B. | ③⑤⑦ | C. | ①②⑤⑦ | D. | 除⑥以外、 |
分析 本题考查学生对物理变化和化学变化的确定.判断一个变化是物理变化还是化学变化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成其他物质的是物理变化
解答 解:①变色不一定是化学变化,例如氧气变为液氧,属于物理变化; ②发光不一定是化学变化,例如灯泡发光放热,属于物理变化; ③燃烧一定是化学变化,属于物质与氧气发生的剧烈的氧化反应; ④爆炸不一定是化学变化,例如轮胎爆炸属于物理变化; ⑤铁生锈生成了主要成分是氧化铁的新物质,属于化学变化; ⑥工业制氧气是利用沸点不同,进行混合物的分离,属于物理变化; ⑦绿色植物通过光合作用获得氧气有新物质氧气、有机物生成,属于化学变化.
故选B.
点评 搞清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在变化中有没有生成其他物质.一般地,物理变化有物质的固、液、气三态变化和物质形状的变化.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
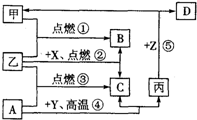 如图所示是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态,化合物D的水溶液呈浅绿色.
如图所示是初中化学中常见物质间的转化关系,其中甲、乙为气态单质,丙为固态单质;A、B、C均为氧化物,常温下B为液态,化合物D的水溶液呈浅绿色.查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是通电电解水的实验装置图.请回答:
如图是通电电解水的实验装置图.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在氧气中燃烧 2Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 化合反应 | |
| B. | 比较铜和银的活动性 Cu+2AgCl═CuCl2+2Ag 置换反应 | |
| C. | 用稀硫酸除铁锈 Fe2O3+2H2SO4═2FeSO4+3H2O 复分解反应 | |
| D. | 除去氧化钙中的碳酸钙 CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ 分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
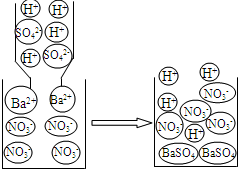 归纳总结是学习化学的重要方法.请回答下列问题:
归纳总结是学习化学的重要方法.请回答下列问题:| 物质 | 镁与冷水 | 铁与冷水 | 铁与水蒸气 | 铜与冷水 | 铜与水蒸气 |
| 反应情况 | 缓慢反应 | 不反应 | 能反应 | 反应 | 不反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
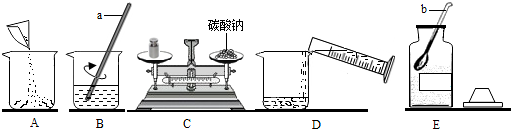
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
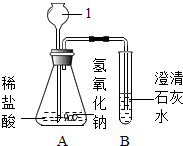 氢氧化钠溶液如果敞口放置容易变质.小明想了解其变质情况,设计如图装置进行实验.
氢氧化钠溶液如果敞口放置容易变质.小明想了解其变质情况,设计如图装置进行实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com