
【题目】为测定由盐酸和硫酸组成的某混合酸中溶质的质量分数,取100g该混合酸,逐滴滴加某Ba(OH)2溶液,生成沉淀BaSO4的质量和pH的变化关系如图1所示.
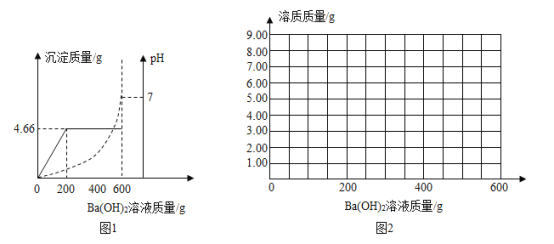
(1)当加入的氢氧化钡溶液为______g时,混合酸恰好被中和.
(2)求Ba(OH)2溶液中的溶质质量分数是多少?_____(写出计算过程,结果精确到0,01%)
(3)盐酸的溶质质量分数是______.(结果精确到0.01%)
(4)请在图2中画出向100g该混合酸中加入600g Ba(OH)2溶液的过程中,混合酸中,生成溶质的质量与所加的Ba(OH)2溶液的质量关系图._____
【答案】(1)600;(2)1.71%;(3)2.92%;(4)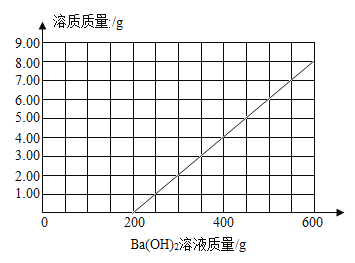
【解析】
向盐酸和硫酸的混酸中滴加氢氧化钡溶液,氢氧化钡先和硫酸反应生成硫酸钡沉淀和水,待硫酸反应完后,氢氧化钡再和盐酸反应生成氯化钡和水。
(1)由图示可知,当加入的氢氧化钡溶液为600g时,pH值等于7,混合酸恰好被中和;
(2)由图示可知,生成沉淀的最大量为4.66g,
设恰好完全反应时,消耗Ba(OH)2的质量为x,
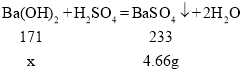
![]()
x=3.42g
Ba(OH)2溶液的溶质质量分数是:![]() ×100%=1.71%;
×100%=1.71%;
(3)设盐酸的溶质质量分数是y,生成氯化钡质量为z
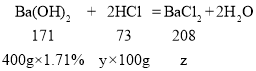
![]()
y=2.92%
z=8.32g
答:盐酸的溶质质量分数是2.92%;
(4)通过上面的反应原理可知氢氧化钡和硫酸反应生成硫酸钡沉淀和水,开始不会生成溶质,盐酸和氢氧化钡反应生成氯化钡和水,溶质质量不断增加,待盐酸反应完后,生成溶质的质量不变,所以得到图像为:



 53随堂测系列答案
53随堂测系列答案科目:初中化学 来源: 题型:
【题目】工业上用闪锌矿(主要成分是ZnS、FeS)冶炼锌,主要流程如下:
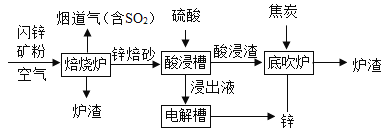
焙烧炉中,ZnS转化为ZnO:2ZnS+ 3O2=2ZnO+2SO2。
(1)酸浸渣的主要成分是铁酸锌(ZnFe2O4),其中铁元素的化合价为____________,铁酸的化学式___________。
(2)酸浸渣的主要成分是铁酸锌(ZnFe2O4)。底吹炉中,主要发生如下反应:
①3ZnFe2O4+C![]() 2Fe3O4+3ZnO+CO↑
2Fe3O4+3ZnO+CO↑
②ZnFe2O4+CO![]() 2FeO+ZnO+CO2
2FeO+ZnO+CO2
③在高温条件氧化锌和一氧化碳反应生成锌蒸汽。
反应①~③中,化合价发生改变的元素有___________,写出反应③的化学方程式____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
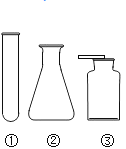
【题目】以下是实验室常用部分仪器:
![]()
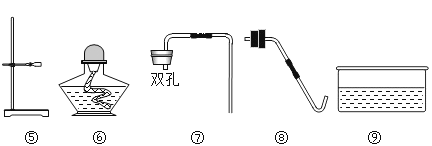
(1)图中仪器④的名称是:____________ ;
(2)小李同学选择仪器制取并收集氧气,他使用了仪器②③④⑨,那么他还需要使用上图中的___________填序号);该发生装置检查气密性的方法是:关闭④的活塞,把导管的一端浸在水里,用手紧贴锥形瓶外壁,若导管口有____________,则说明该装置不漏气。
(3)小张同学正在收集一瓶 CO2, 不知是否收集满了,其验满方法是___________。
(4)小王选用上述仪器,用锌粒和稀硫酸制氢气,锌粒反应完后,发现还有较多的灰黑色固体物质,从反应后的混合物中分离得到该灰黑色固体的操作方法是____________。
(提出问题)灰黑色固体物质的成分是什么呢?
(提出猜想)可能含有单质碳
(设计实验)请设计实验用化学方法证明该灰黑色固体物质中是否含有单质碳。
实验方法 | 现象和结论 |
________________ | ________________ |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活中常见物质的性质、制法是化学研究的重要内容。
(1)复分解反应发生的条件是_____。
(2)m克氢氧化钠与一定量的稀盐酸恰好完全反应,若改用等质量的氢氧化钙去中和相同的稀盐酸,则溶液的pH_____7。(填等于、大于或小于)
(3)氢氧化钠敞口放到空气中会变质,请写出氢氧化钠变质的化学反应方程式_____。
(4)下图装置可做一氧化碳还原氧化铁的实验。
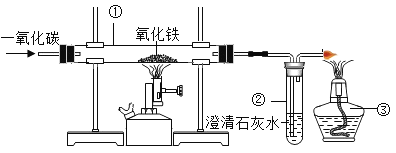
①硬质试管①中的实验现象为_____;
②该实验中发生化合反应的化学方程式为_____;
③工业上用高炉来炼铁,向高炉中加入铁矿石、焦炭和石灰石,并鼓入大量空气,那么高炉炼铁时焦炭的作用为:_____和_____
(5)在实验室称取20g赤铁矿样品置于烧杯中(杂质不参加反应),加入100g溶质质量分数为21.9%的盐酸,二者恰好完全反应。试计算样品中氧化铁的质量分数_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是初中化学做过的一些实验,回答有关问题.
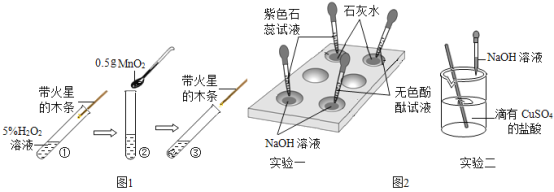
(1)图1是分解H2O2中MnO2作用的探究实验.
步骤①的现象说明常温下过氧化______(填“易分解”或“不易分解”);步骤③反应结束后向试管中加入5%H2O2溶液,伸入带火星的木条,木条______,说明二氧化锰的化学性质没有改变;接着还要完成的实验是______.
(2)在《酸、碱的化学性质》实验中,我们进行过下列一些实验(如图2),回答相关问题:
①实验一选在白色点滴板上进行的优点是______.
②实验二设计的目的是在不使用指示剂的情况下也能证明酸和碱之间能够发生______,当观察到______时,证明酸碱之间的反应已经完成.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(7分)下列是小明同学配制100 g 10% NaCl溶液的实验操作示意图。
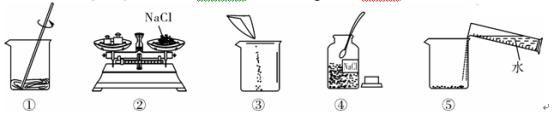
(1)该实验正确的操作顺序是____________(填序号)。
(2)认真观察指出图中错误的操作步骤________(填序号)。
(3)配制该溶液需要NaCl固体________g,需要水________mL(ρ水=1 g/mL)。
(4)小明同学将称量完毕的食盐转移到烧杯里时,不慎将少量食盐洒落在桌面上,这样会使所配制的溶液中溶质质量分数________10%(填“>”“=”或“<”)。
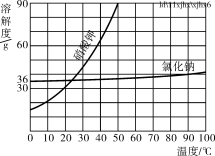
(5)部分物质溶解度曲![]() 线如右图所示,在20 ℃时,将40 g NaCl固体加入到100 g水中,搅拌使其充分溶解,你认为所得NaCl溶液的质量是________g,溶质质量分数是________%(精确到0.1%)。
线如右图所示,在20 ℃时,将40 g NaCl固体加入到100 g水中,搅拌使其充分溶解,你认为所得NaCl溶液的质量是________g,溶质质量分数是________%(精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是家用豆浆机,请根据图回答下列问题:
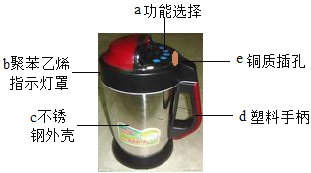
(1)属于有机合成材料的是______(填物质编号);
(2)豆浆中含有的最丰富的营养物质是______;
(3)传统的生豆浆是用石磨来打磨的,打磨的过程属于______变化;
(4)用操作将黄豆渣分离的方法类似于我们实验中的______操作;
(5)金属在生活生产中有重要的应用.某化学兴趣小组向硝酸银、硝酸铜、硝酸镁的混合溶液中加入一定质量的锌,充分反应后过滤,得到滤渣A和滤液B.请回答下列问题:
Ⅰ.若反应前后溶液质量不变,A中一定含有______.
Ⅱ.若反应后溶液质量减少,B中一定含有的金属离子是____,不能确定的金属离子是____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钛和钛合金是21世纪的重要材料,具有很多优良性能。钛元素在化合物中一般显+4价,它在元素周期表中的部分信息见下图.下列说法中错误的是( )
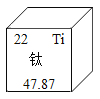
A.钛元素原子的质子数为22
B.钛元素属于金属元素
C.钛元素的相对原子质量为47.87g
D.钛元素与氯元素组成的化合物化学式为TiCl4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)Mg与NH4Cl溶液反应,除生成一种盐外,还有气泡产生。为确定气体的成分,进行下列实验探究:
【假设与猜想】气体可能是HCl,NH3,H2中的一种或几种。
【查阅资料】
①NH3+HCl=NH4Cl ②NH3+H2SO4= (NH4)2SO4 ![]()
【实验探究】
(1)为确定是否含有HCl,将气体通入酸化的 溶液中,无沉淀产生,则该气体中无HCl。
(2)为了探究其他气体是否存在,又设计了如下实验装置:
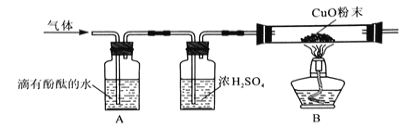
①A中观察到 ,证明有NH3;
②B中玻璃管内观察到____________证明有H2;
③浓硫酸的作用是________________。
【实验结论】Mg与NH4Cl溶液反应生成盐,NH3和H2 。写出化学方程式 。
【实验反思】综合以上信息和实验结论,有同学认为不需要单独检验HCl,就能证明HCl不存在。请评价这种说法是否合理 (填“是”或“否”),理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com