

分析 (1)根据碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠进行分析;
(2)根据碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,依据碳酸钠的质量计算生成碳酸钙的质量;
(3)根据化学方程式计算出混合物中氯化钙的质量,计算混合物中各成分的质量比;
(4)根据烧杯中发生的反应进行分析;
(5)根据反应后溶液的质量和溶质的质量进行计算.
解答 解:(1)碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,化学方程式为:CaCl2+Na2CO3=CaCO3↓+2NaCl;
(2)设生成碳酸钙沉淀质量为x,参加反应的氯化钙质量为y,生成氯化钠质量为z,
CaCl2+Na2CO3=CaCO3↓+2NaCl
111 106 100 117
y 100g×10.6% x z
$\frac{111}{y}$=$\frac{106}{100g×10.6%}$=$\frac{100}{x}$=$\frac{117}{z}$
x=10g
y=11.1g
z=11.7g
(3)所以混合物中碳酸钙质量为:16.1g-11.1g=5g,各成分质量比是:11.1g:5g=111:50;
(4)通过分析题中的反应可知,在加入碳酸钠溶液的过程中,烧杯中溶质质量的变化情况为:氯化钙的质量逐渐减少至消失,氯化钠的质量逐渐增多;
(5)设需要加水质量为:$\frac{11.7g}{5%}$=234-100g-100g×(1-10.6%)-11.7g=32.9g.
故答案为:(1)CaCl2+Na2CO3=CaCO3↓+2NaCl;
(2)$\frac{106}{100g×10.6%}$=$\frac{100}{x}$;
(3)111:50;
(4)氯化钙的质量逐渐减少至消失,氯化钠的质量逐渐增多;
(5)32.9g.
点评 不同主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | +3 | B. | +5 | C. | +6 | D. | +7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
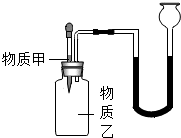 下列字母A~G表示9初中化学常见的物质,它们由H、C、O、Cl、Ca中的2~3种元素组成.
下列字母A~G表示9初中化学常见的物质,它们由H、C、O、Cl、Ca中的2~3种元素组成.| 序号 物质 | ① | ② | ③ | ④ |
| 物质甲 | 盐酸 | 过氧化氢溶液 | 水 | 过氧化氢溶液 |
| 物质乙 | 碳酸钙 | 二氧化锰 | 氧化钙 | 氧化钙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com