
| 步骤 | 现象 | 结论 |
| 取少量溶液a,滴加氯化铜溶液 | (26)溶液中无蓝色絮状沉淀 | 不含氢氧化钠 |
| 方案 | 步骤 | 现象 |
| 一 | 取少量溶液a,滴加硝酸银溶液 | 产生白色沉淀 |
| 二 | 取少量溶液a,加入镁粉 | 产生气泡 |
| 液体 | 步骤 | 现象 |
| 水 | 打开分液漏斗活塞,加入液体后关闭活塞 | D中导管现有气泡冒出,后D中导管无明显现象 |
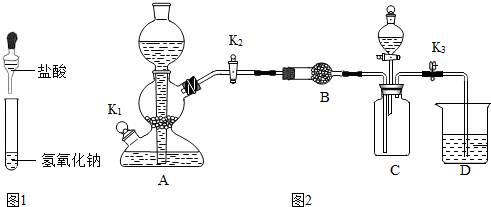
分析 ①氢氧化钠和盐酸反应生成氯化钠和水,根据是否完全中和以及反应物是否剩余来分析;
氢氧化钠溶液能与氯化铜溶液反应产生蓝色的氢氧化铜沉淀;
根据检验氯离子的方法以及反应的过程来分析;
②根据二氧化碳的性质来分析;根据无水硫酸铜易与水反应生成五水硫酸铜来分析;根据启普发生器的使用原理来分析;找一种和二氧化碳不会反应(或者反应微弱)的即可,进而证明倒吸是因为二氧化碳和氢氧化钠反应造成的.
解答 解:①氢氧化钠和盐酸反应生成氯化钠和水,若二者恰好完全反应,则溶质是有氯化钠,若氢氧化钠有剩余,则溶质为氯化钠和氢氧化钠,若盐酸有剩余,则溶质为氯化钠和氯化氢;故填:NaOH+HCl=NaCl+H2O;3;
Ⅰ、若含有氢氧化钠,则加入氯化铜溶液后会产生氢氧化铜蓝色絮状沉淀,故填:溶液中无蓝色絮状沉淀;
Ⅱ、检验溶液中是否含有氯化氢,不能用硝酸银溶液,因为硝酸银溶液能与溶液中的氯化钠反应产生白色沉淀;故填:方案一不合理,生成的氯化钠也会与硝酸银生成白色沉淀;
若溶液中加入镁粉产生气体,则说明含有盐酸,故填:溶液中含有稀盐酸,且溶质是氯化钠和氯化氢;
将溶液蒸发结晶,即可得到纯净的氯化钠晶体,故填:蒸发结晶;
②Ⅰ、C中若收集满了二氧化碳,则二氧化碳会进入D装置与水反应生成碳酸,碳酸能使紫色的石蕊试液变红色;故填:红;
Ⅱ、白色的硫酸铜粉末与水反应生成蓝色的硫酸铜晶体,故填:CuSO4+5H2O=CuSO4•5H2O;
Ⅲ、二氧化碳收集满后,应将K2关闭,故填:关闭K2;
Ⅴ、二氧化碳和氢氧化钠反应生成碳酸钠和水,但是二氧化碳和水反应非常微小(可以不于考虑).这样一比较可以发现,倒吸是有二氧化碳和氢氧化钠反应造成的;
故填:水;D中导管现有气泡冒出,后D中导管无明显现象;
氢氧化钠与二氧化碳反应生成碳酸钠和水,故填:2NaOH+CO2=Na2CO3+H2O.
点评 本题通过实验探究,考查了氢氧化钠的性质,掌握氢氧化钠的化学性质以及有关化学方程式的书写是解题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 反应消耗3molY | B. | X可能含有三种元素 | ||
| C. | M属于有机物 | D. | X和N的物质的量的比为1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
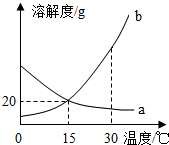 a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )| A. | 15℃时,a、b 的溶解度均为20g | |
| B. | 加水或升温均可使b的饱和溶液变为不饱和溶液 | |
| C. | 将 30℃时a的饱和溶液降温至15℃,溶质的质量分数不变 | |
| D. | 20℃时分别向100g 水中加入20ga和 b,升温至30℃,所得溶液均为饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 香槟酒含有大量由糖分分解成的酒精和碳酸.如图是打开香槟酒一瞬间的情景.
香槟酒含有大量由糖分分解成的酒精和碳酸.如图是打开香槟酒一瞬间的情景.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com