解:
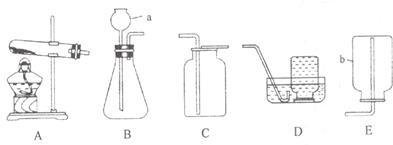
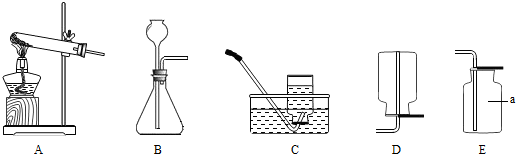
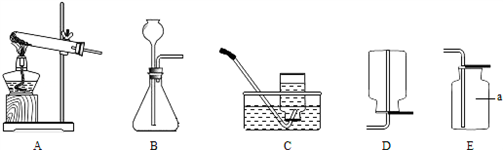
(1)①实验室制取二氧化碳用大理石与稀盐酸反应,不需加热,所以选择发生装置B,二氧化碳的密度比空气大且能溶于水,所以只能用向上排空气法收集;制取二氧化碳的装置适用于固体和液体不需加热制取气体且气体的密度比空气大的气体,实验室用双氧水分解,二氧化锰作催化剂的方法制取氧气符合此条件,故该装置还可用于双氧水制取氧气;双氧水分解生成水和氧气,方程式是2H
2O
2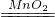
2H
2O+O
2↑;
故答案为:
B和C; O
2; 2H
2O
2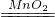
2H
2O+O
2↑;
②由于CO
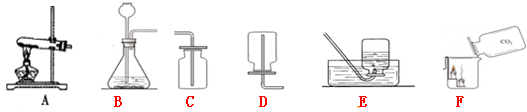
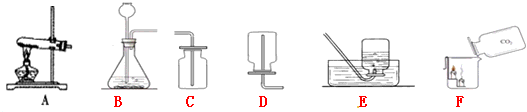
2不能燃烧,也不支持燃烧,密度比空气大,所以向烧杯中倾倒二氧化碳,可观察到的现象是下层蜡烛先熄灭,上层蜡烛后熄灭;通过此现象也证明了二氧化碳的这一性质;
故答案为:
下层蜡烛先熄灭,上层蜡烛后熄灭; CO
2不能燃烧,也不支持燃烧;密度比空气大.
③若采用加热固体碳酸氢钠的方法制取二氧化碳,需要加热,故选发生装置A;之所以不用加热碳酸氢铵的方法制取,是因为该反应除了生成二氧化碳,还生成氨气,使所收集的气体不纯;
故答案为:
A; 生成物中有其它气体,制得的CO
2不纯;
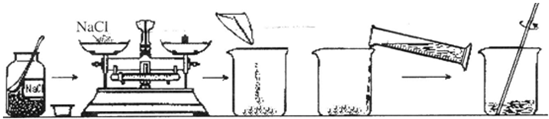
(2)①根据溶质的质量分数计算方法,小华同学应称取氯化钠的质量是100g×20%=20g;
故答案为:20g;
②取用药品时,瓶塞应倒放,不能正放;
故答案为:瓶塞正放了;
③称取食盐的过程中,发现指针偏向分度盘右侧,说明称量的药品不足,应继续添加药品;
故选C;
④配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能原因有溶质的质量不足或溶剂的量多了;如称量前天平没有调平或称量纸上残留少量食盐,用量筒量取水时俯视液面等;
故答案为:称量前天平没有调平或称量的纸上残留少量食盐(合理即可).
分析:(1)①根据实验室制取二氧化碳的反应物和反应条件选择发生装置,依据二氧化碳的密度和溶解性选择收集装置;依据制取二氧化碳的装置的适用范围进行分析,选择还可用此装置制取的气体,并依据反应原理书写方程式;
②根据二氧化碳的相关性质分析解答;
③依据发生装置的选择依据进行分析;并对反应原理进行分析,得出正确的结论;
(2)①溶质的质量=溶液的质量×溶质的质量分数;
②根据仪器的使用注意事项进行分析;
③称取食盐的过程中,发现指针偏向分度盘右侧,说明称量的药品不足;
④配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能原因有溶质的质量不足或溶剂的量多了.
点评:本题考查知识综合、细致,对实实验室制取气体的装置选取、反应原理、气体的性质等知识进行了考查,同时考查了溶液配制的有关知识,能很好的考查出学生对相关知识的掌握和应用能力.

 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑ NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑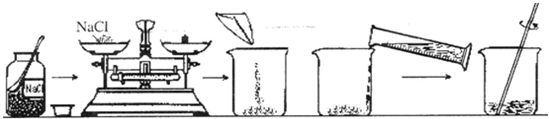
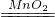 2H2O+O2↑;
2H2O+O2↑;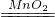 2H2O+O2↑;
2H2O+O2↑;