
| A. | “灭火弹”灭火的主要原理是降低燃烧物的着火点 | |
| B. | 液态四氯化碳转化为气态时分子间的间隔变大 | |
| C. | 四氯化碳不能燃烧也不支持燃烧 | |
| D. | 气态四氯化碳的密度比空气大 |
科目:初中化学 来源: 题型:实验探究题
| 时间 (min) 浓度 条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 预计现象 | 预计结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液 | 猜想(B)正确 | |
| 猜想(C)正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
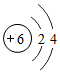 ,该元素原子核内有6个质子,最外层有4个电子.
,该元素原子核内有6个质子,最外层有4个电子.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
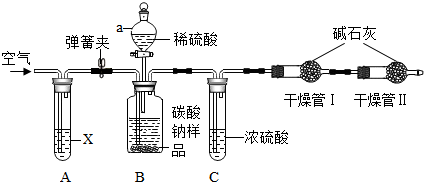
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com