
【题目】两会“实名制”矿泉水亮相,服务员们“沏茶倒水”的场景不再出现,取而代之的是为每名委员提供一瓶矿泉水,而且每瓶矿泉水上还贴有委员名字。下列说法不正确的是

A. 这种做法是倡导节俭新风
B. 水是人体所需营养物质之一
C. 矿泉水中的钙、锌、铁、硒都属于人体需要的微量元素
D. 罐装矿泉水的塑料瓶子由有机高分子材料制作而成
科目:初中化学 来源: 题型:
【题目】已知A、B为两种黑色粉末,D为红色单质.A、B、C、D、E、F 五种物质之间的转化关系如图所示.(部分生成物已省略).请回答:
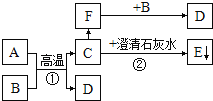
(1)A的化学式为 ,D的化学式为 ;A和B反应的化学方程式为 .
(2)反应②的化学方程式为 ,在上述反应中A、F都具有 (填“氧化性”或“还原性”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)为延长食品保质期,常在食品中添加苯甲酸(C6H5COOH)作为防腐剂。回答下列问题:①苯甲酸是由 种元素组成;②苯甲酸中碳元素与氢元素的质量比为 (最简整数比)。
(2)小明称取黄铜(铜锌合金)样品10.0克,再用100.0克稀硫酸溶液逐滴滴入,测得实验数据如图所示。

求:
①该铜锌合金中,铜和锌的质量比是 (最简整数比)。
②所用稀硫酸溶液中溶质的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 海水“晒盐”后剩余的母液(苦卤)一定是食盐的饱和溶液
B. 蒸发结晶食盐时,待水分全部蒸发,才能停止加热
C. 利用多次蒸发结晶的方法可去除粗盐中的可溶性杂质
D. 海底蕴藏着无以计数的能源,所以我们不用担心未来能源问题
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是几种常见的实验室制取气体的实验装置。请回答:
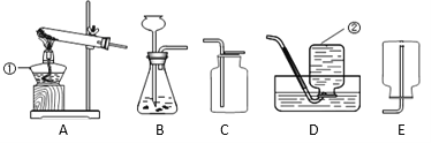
(1)指出图中标号仪器的名称:② __________。
(2)若用A装置作为高锰酸钾制取氧气的发生装置,存在的缺点是______。
(3)若用A装置中的酒精灯改为酒精喷灯进行木炭还原氧化铜的实验,写出该反应的化学方式 __________________________。
(4)实验室用B装置制取的二氧化碳通入澄清的石灰水用化学方程式表示为 ________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像,如图所示。下列说法正确的是

A. 图中c点所示溶液呈碱性
B. 图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4
C. 该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中
D. 由a点到b点的pH变化过程证明酸和碱发生了中和反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班同学在做《基础实验8》中碱的化学性质时,发现将NaOH固体溶于水后的溶液与CuS04溶液反应时出现了三种实验现象:蓝色絮状沉淀、浅绿色沉淀、亮蓝色溶液。产生蓝色絮状沉淀时的反应方程式为_______________________________________。对于异常实验现象,
同学们展开研究性学习。
【提出问题】实验中产生异常现象的原因是什么?
【初步探究】甲同学将饱和硫酸铜溶液逐滴加到5mL饱和氢氧化钠溶液中。实验现象如下:
滴加CuSO4溶液的量 | 实验现象 |
第1~6滴 | 产生蓝色沉淀,振荡后沉淀消失,形成亮蓝色溶液。 |
第7~9滴 | 产生蓝色沉淀,振荡后沉淀不消失,沉淀逐渐增多。 |
第10~20滴 | 蓝色沉淀不再增加,振荡后沉淀逐渐变为浅绿色。 |
【实验结论】_____________________________是实验出现“异常”的主要因素。
【再次探究】两种异常现象产物是什么?
【查阅资料】
①碱式硫酸铜是一种浅绿色固体,化学式可表示为aCuSO4·bCu(OH)2难溶于水,在酸溶液中可发生反应生成Cu2+、SO42—和H2O。加热时能分解生成氧化铜、非金属氧化物和氧气。
②铜酸钠[Na2Cu(OH)4]能溶于水,溶液呈亮蓝色。该溶液不稳定,久置或加热易生成氧化铜沉淀。
③碱式硫酸铜、氢氧化铜、铜酸钠之间可逐步转化。
【猜想假设】
Ⅰ.Cu(OH)2在NaOH溶液中溶解生成铜酸钠。
Ⅱ.实验中形成浅绿色沉淀是碱式硫酸铜。
【实验探究】
Ⅰ.乙同学向Cu(OH)2中加入过量饱和NaOH溶液,沉淀溶解,滴加少量稀硫酸,出现黑色沉淀。
Ⅱ.丙同学取出实验中浅绿色固体,分成等质量两份,一份高温灼烧后只得到1.6gCuO固体,另一份滴加10%的稀盐酸至恰好完全反应,共用去盐酸10.95g。
【结论解释】猜想Ⅰ成立。出现黑色沉淀原因是________________________________。
猜想II成立。a:b=________________。
【实验反思】丁同学按照书本要求向2mLCuSO4溶液中逐滴加入稀氢氧化钠溶液,始终未形成亮蓝色溶液,说明实验现象还与______________________有关,实验时要遵守实验要求。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在密闭容器内进行的某反应中,测得反应前(t0)、反应中(t1)、反应后(t2)不同时刻甲、乙、丙、丁四种物质的质量分数分别如下图所示,则下列说法不正确的是
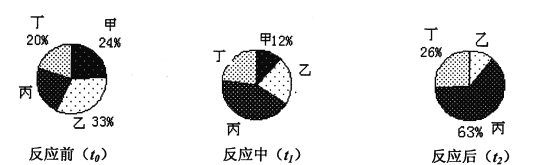
A. t1时刻,乙、丁、丙所占的质量分数分别为22%、23%和43%
B. 若反应前甲、乙、丙、丁四种物质的总质量为100克,则再增加12克甲,甲与乙则恰好
C. 该反应既不可能是化合反应,也不可能是分解反应
D. 若甲和丁分别是镁和碳,则该反应中甲和丁的化学计量数之比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com